题目内容
在298K、100kPa下,将氯气溶于水形成饱和溶液.请回答下列问题:
(1)该反应的离子方程式为 ;
(2)在上述平衡体系中加入少量NaCl固体,平衡将向 移动;
(3)如果增大氯气的压强,氯气在水中的溶解度将 (填“增大”“减小”或“不变”),平衡将 移动.(1分)(填“向左”“向右”或“不”)
(4)若要增加c(HClO),可采取的措施有
a、加水 b、加NaOH固体 c、加Na2CO3固体 d、再通入Cl2.
(1)该反应的离子方程式为
(2)在上述平衡体系中加入少量NaCl固体,平衡将向
(3)如果增大氯气的压强,氯气在水中的溶解度将
(4)若要增加c(HClO),可采取的措施有
a、加水 b、加NaOH固体 c、加Na2CO3固体 d、再通入Cl2.
考点:氯气的化学性质,化学平衡的影响因素
专题:化学平衡专题
分析:(1)氯气和水之间反应生成盐酸和次氯酸;
(2)增大产物浓度,化学平衡向着逆反应方向进行;
(3)增大压强,化学平衡向着气体系数和减小的方向进行;
(4)若要增加c(HClO),可以采取使化学平衡正向移动的措施,但是加的物质不和次氯酸之间反应.
(2)增大产物浓度,化学平衡向着逆反应方向进行;
(3)增大压强,化学平衡向着气体系数和减小的方向进行;
(4)若要增加c(HClO),可以采取使化学平衡正向移动的措施,但是加的物质不和次氯酸之间反应.
解答:
解:(1)氯气和水之间反应生成盐酸和次氯酸,该反应的离子方程式为:Cl2+H2O?H++Cl-+HClO,故答案为:Cl2+H2O?H++Cl-+HClO;
(2)在上述平衡体系中加入少量NaCl固体,增大产物氯离子浓度,化学平衡向着逆反应方向进行,故答案为:左;
(3)增大压强,化学平衡向着气体系数和减小的方向进行,即正向进行,氯气在水中的溶解度将增大,故答案为:增大;向右;
(4)a、加水会使得次氯酸浓度减小,故a错误;
b、加NaOH固体,会消耗次氯酸,会使得次氯酸浓度减小,故b错误;
c、加Na2CO3固体,会消耗次氯酸,会使得次氯酸浓度减小,故c错误;
d、再通入Cl2,会使得平衡正向移动,次氯酸浓度增大,故D正确.
故选d.
(2)在上述平衡体系中加入少量NaCl固体,增大产物氯离子浓度,化学平衡向着逆反应方向进行,故答案为:左;
(3)增大压强,化学平衡向着气体系数和减小的方向进行,即正向进行,氯气在水中的溶解度将增大,故答案为:增大;向右;
(4)a、加水会使得次氯酸浓度减小,故a错误;
b、加NaOH固体,会消耗次氯酸,会使得次氯酸浓度减小,故b错误;
c、加Na2CO3固体,会消耗次氯酸,会使得次氯酸浓度减小,故c错误;
d、再通入Cl2,会使得平衡正向移动,次氯酸浓度增大,故D正确.
故选d.
点评:本题考查学生氯气和水反应的化学平衡的移动知识,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
下列各组物质中,所含分子数相同的是( )
| A、10g H2和10g O2 |
| B、5.6LN2(标准状况)和11g CO2 |
| C、18g H2O和0.5mol Br2 |
| D、224mL H2(标准状况)和0.1mol N2 |
 某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述不正确的是( )
某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述不正确的是( )A、断开K2,闭合K1时,总反应的离子方程式为:2H2O+2Cl-
| ||||
| B、断开K2,闭合K1时,铜电极产生的气体略多于石墨 | ||||
| C、断开K1,闭合K2时,铜电极上的电极反应为:H2-2e-=2 H+ | ||||
| D、断开K1,闭合K2时,溶液中的Na+向石墨电极迁移 |
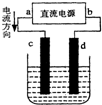 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )| A、a为负极、d为阳极 |
| B、将淀粉KI试纸的玻璃棒靠近d处一段时间会变蓝色 |
| C、电解过程中转移0.2mol电子,d电极质量增加6.4克 |
| D、电解过程中,铜离子向C极移动 |
 由于催化剂可以为化学工业生产带来巨大的经济效益,催化剂研究和寻找一直是受到重视的高科技领域.
由于催化剂可以为化学工业生产带来巨大的经济效益,催化剂研究和寻找一直是受到重视的高科技领域.
