题目内容
13.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 56gFe与1 molCl2充分反应转移电子数为3NA | |
| B. | 常温常压下,22 g D3O+含有10 NA个电子 | |
| C. | 25℃时,1 L pH=12的Ba(OH)2溶液中含有的OH-的数目为0.02 NA | |
| D. | 1 L0.1 mol/L Na2CO3溶液中CO32-和HCO3-总数为0.1NA |
分析 A、56g铁和1mol氯气反应,铁过量;
B、求出D3O+的物质的量,然后根据1mol中D3O+含10mol电子来分析;
C、pH=12的氢氧化钡溶液中,氢氧根的浓度为0.01mol/L;
D、CO32-在溶液中会部分水解为CO32-、H2CO3.
解答 解:A、56g铁和1mol氯气反应,铁过量,而氯气反应后变为-1价,故1mol氯气转移2mol电子即2NA个,故A错误;
B、22gD3O+的物质的量为$\frac{22g}{22g/mol}$=1mol,而1mol中D3O+含10mol电子,故含10NA个,故B正确;
C、pH=12的氢氧化钡溶液中,氢氧根的浓度为0.01mol/L,故1L溶液中氢氧根的个数为0.01NA个,故C错误;
D、CO32-在溶液中会部分水解为CO32-、H2CO3,根据物料守恒可知,溶液中H2CO3、CO32-和HCO3-总数为0.1NA,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
4.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 1molFeCl3水解生成的Fe(OH)3胶粒数为1NA | |
| B. | 4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5NA | |
| C. | 标准状况下,11.2LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 1mol•L-1AlCl3溶液中含有3NA个Cl- |
1.最近中美研究人员发明了一种可快速充电放电的铝离子电池,该电池电解质为离子液体,离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液,放电过程中不产生其他离子且有机阳离子不参与电极反应,放电时有关离子转化如图所示,下列说法正确的是( )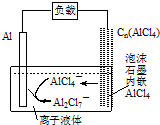

| A. | 放电时,负极发生:2AlCl4--e-=Al2Cl7-+Cl- | |
| B. | 放电时,电路中每流过3mol电子,正极减少27g | |
| C. | 充电时,泡沫石墨极与外电源的负极相连 | |
| D. | 充电时,阴极发生:4Al2Cl7-+3e-=Al+7AlCl4- |
8.下列粒子属等电子体的是( )
| A. | NO和O2 | B. | CH4和NH4+ | C. | N2H4和H2O2 | D. | HCl和H2O |
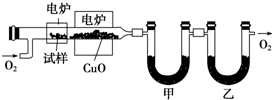
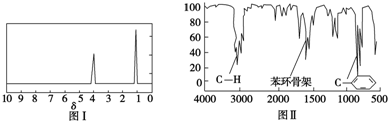

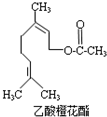 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( ) CH4(g)+H2O(g)△H=-203kJ•mol-1.
CH4(g)+H2O(g)△H=-203kJ•mol-1.