题目内容
3.短周期主族元素X、Y、Z、R原子序数依次增大且最外层电子数之和为18.Y、R同主族,短周期中Z原子半径最大,Y最外层电子数是次外层的3倍.下列推断正确的是( )| A. | 化合物Z2R2中只含有离子键不含共价键 | |
| B. | 元素Y的简单气态氢化物的热稳定性比R弱 | |
| C. | 离子半径从大到小的顺序为R>Z>X>Y | |
| D. | 一定条件下,Y单质可以将X单质从其氢化物中置换出来 |
分析 短周期中Z原子半径最大,Z为Na元素,Y最外层电子数是次外层的3倍,应为O元素,Y、R同主族,则R为S元素,短周期主族元素X、Y、Z、R原子序数依次增大且最外层电子数之和为18,可知X的最外层电子数为18-6-6-1=5,可知X为N元素,以此解答该题.
解答 解:短周期中Z原子半径最大,Z为Na元素,Y最外层电子数是次外层的3倍,应为O元素,Y、R同主族,则R为S元素,短周期主族元素X、Y、Z、R原子序数依次增大且最外层电子数之和为18,可知X的最外层电子数为18-6-6-1=5,可知X为N元素,
A.化合物Na2S2结构类似过氧化钠,含有共价键,故A错误;
B.非金属性O>S,元素的非金属性越强,对应的氢化物越稳定,故B错误;
C.O和Na的离子具有相同的核外电子排布,核电荷数越大离子半径越大,故C错误;
D.氨气在氧气中燃烧可生成氮气和水,故D正确.
故选D.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、原子结构推断元素为解答该题的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 金属钠取用时要用镊子.多余的钠不能放回瓶中 | |
| B. | 用pH试纸检验气体时应预先润湿 | |
| C. | 用苯苹取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | 可用新制的银氨溶液鉴别两瓶失去标签的乙醛和葡萄糖溶液 |
11.把SO2通入NaOH溶液中,当SO2和NaOH完全反应时,其质量比为6:5,则下列说法正确的是( )
| A. | 反应后SO2有剩余 | |
| B. | 溶液还可吸收SO2 | |
| C. | 溶液中除OH-外,只存在一种阴离子 | |
| D. | 溶液中溶质(正盐与酸式盐)的物质的量之比为2:1 |
18.氧族元素的氢化物的沸点如表:
下列关于氧族元素氢化物的沸点高低的分析和推断中,正确的是( )
| H2O | H2S | H2Se | H2Te |
| 100℃ | -60.75℃ | -41.5℃ | -1.8℃ |
| A. | 氧族元素氢化物沸点高低与范德华力的大小无关 | |
| B. | 范德华力一定随相对分子质量的增大而减小 | |
| C. | 水分子间可能还存在一种特殊的分子间作用力 | |
| D. | 水分子间存在共价键,加热时较难断裂 |
8.下列关于元素周期表的叙述中,不正确的是( )
| A. | 有七个周期,十八个族 | B. | 是元素周期律的具体表现形式 | ||
| C. | 对工农业生产有一定的指导作用 | D. | 是学习和研究化学的重要工具 |
15.人大量喝水时,胃液pH变化的正确图象是( )
| A. | 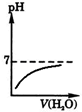 | B. |  | C. | 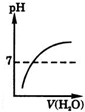 | D. | 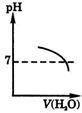 |
12.食用下列物质不会引起中毒的是( )
| A. | 加碘盐(含碘酸钾的食盐) | B. | 用含有铜锈的器皿盛装酸性食物 | ||
| C. | 用于混凝土防冻的亚硝酸钠 | D. | 用碳酸钡作X射线透视的“钡餐” |
13.下列物质中,不属于合金的是( )
| A. | 不锈钢 | B. | 黄铜 | C. | 生铁 | D. | 水银 |