题目内容
13.实验室常用CS2溶解硫磺(S8)或白磷(P4),下列推测错误的是( )| A. | CS2是非极性分子 | B. | CS2的沸点高于CO2 | ||
| C. | CS2不能在空气中燃烧 | D. | CS2能证明非金属性S>C |
分析 A.非极性分子的溶质极易溶于非极性分子的溶剂;
B.分子晶体熔沸点与其相对分子质量成正比,还与氢键有关;
C.CS2在空气中燃烧生成二氧化硫和二氧化碳;
D.在同一种化合物中,电负性大的元素显负化合价,电负性小的元素显正化合价,元素的电负性越大其非金属性越强.
解答 解:A.非极性分子的溶质极易溶于非极性分子的溶剂,CS2溶解硫磺(S8)或白磷(P4),硫磺和白磷是非极性分子,根据相似相溶原理知,CS2为非极性分子,故A正确;
B.分子晶体熔沸点与其相对分子质量成正比,还与氢键有关,这两种物质都是分子晶体,且二硫化碳相对分子质量大于二氧化碳,所以CS2的沸点高于CO2,故B正确;
C.CS2在空气中燃烧生成二氧化硫和二氧化碳,所以二硫化碳能在空气中燃烧,故C错误;
D.在同一种化合物中,电负性大的元素显负化合价,电负性小的元素显正化合价,元素的电负性越大其非金属性越强,该化合物中C为+4价、S为-2价,所以非金属性S>C,故D正确;
故选C.
点评 本题考查较综合,涉及相似相溶原理、非金属性强弱判断、熔沸点高低判断等知识点,明确物质结构及其性质、元素周期律等知识点是解本题关键,题目难度不大.

练习册系列答案
相关题目
1.下列叙述错误的是( )
| A. | SO2使品红溶液褪色与Cl2使品红溶液褪色的原理不同 | |
| B. | 利用焰色反应可以鉴别KCl和NaCl | |
| C. | 利用澄清石灰水可以鉴别NaHCO3溶液和Na2CO3溶液 | |
| D. | 用AgNO3溶液和稀硝酸可以鉴别KCl和K2CO3 |
8.下列说法或操作:
①做实验时可用手直接拿取金属钠
②除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
③用酒精可以从饱和碘水中萃取碘
④除去CO中少量O2:通过灼热的Cu网后收集气体
⑤除去K2CO3固体中少量NaHCO3:
置于坩埚中加热.其中正确的是( )
①做实验时可用手直接拿取金属钠
②除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
③用酒精可以从饱和碘水中萃取碘
④除去CO中少量O2:通过灼热的Cu网后收集气体
⑤除去K2CO3固体中少量NaHCO3:
置于坩埚中加热.其中正确的是( )
| A. | ①②③④⑤ | B. | ②④⑤ | C. | ②③④ | D. | 以上都不正确 |
18.在同温同压下用排气法收集NH3和HCl进行喷泉实验(如图),下列说法错误的是(设Vm表示该条件下气体摩尔体积)( )
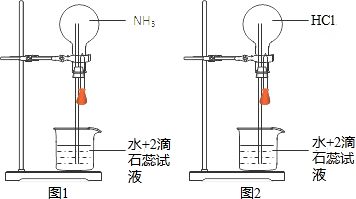

| A. | 所得溶液中溶质的物质的量浓度均为$\frac{1}{{V}_{m}}$mol•L-1 | |
| B. | “喷泉”结束时烧瓶内充满液体 | |
| C. | 图2可通过膨胀法引发“喷泉” | |
| D. | 图1、图2中喷泉的颜色分别为蓝色、红色 |
5.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| C. | 常温常压下,8g O2含有4NA个电子 | |
| D. | 常温常压下,22.4L的NO2和CO2混合气体含有2nA个O原子 | |
| E. | 常温常压下,18 g H2O 中含有的原子总数为3NA | |
| F. | 标准状况下,11.2 L CH3CH2OH 中含有的分子数目为0.5NA | |
| G. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| H. | 28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| I. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| J. | 18g H2O中含的质子数为10NA | |
| K. | 46g NO2和N2O4混合气体中含有原子总数为3NA |
8.金属钠与下列溶液反应时既有沉淀又有气体生成的是( )
| A. | ( NH4 )2SO4 | B. | NaHCO3 | C. | Ba Cl2 | D. | Cu SO4 |
9.下列各组物质,前者逐滴滴加(或逐渐通入)到后者中直至过量,没有出现“先有白色沉淀,后来沉淀又完全消失”现象的是( )
| A. | 盐酸滴入Na[Al(OH)4]溶液中 | B. | CO2气体通入漂白粉溶液中 | ||
| C. | NaOH溶液滴入AlCl3溶液中 | D. | Ba(OH)2溶液滴入Al2(SO4)3溶液中 |
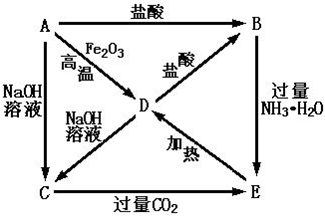 A、B、C、D、E 五种物质存在以下转化关系,已知A 为金属单质,在以下各步反应中E 是白色沉淀.
A、B、C、D、E 五种物质存在以下转化关系,已知A 为金属单质,在以下各步反应中E 是白色沉淀.