题目内容
下列各组离子在溶液中能大量共存的是( )
| A、Na+、Al3+、NO3-、H+ |
| B、Ba2+、Na+、Cl-、SO42- |
| C、Mg2+、H+、SO42-、OH- |
| D、H+、Na+、CO32-、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:A.Na+、Al3+、NO3-、H+离子之间不满足离子反应发生条件;
B.钡离子与硫酸根离子反应生成硫酸钡沉淀;
C.镁离子、氢氧根离子与氢离子反应;
D.氢离子与碳酸根离子反应.
B.钡离子与硫酸根离子反应生成硫酸钡沉淀;
C.镁离子、氢氧根离子与氢离子反应;
D.氢离子与碳酸根离子反应.
解答:
解:A.Na+、Al3+、NO3-、H+离子之间不反应,在溶液中能够大量共存,故A正确;
B.Ba2+、SO42-之间反应生成硫酸钡,在溶液中不能大量共存,故B错误;
C.Mg2+、H+都与OH-反应,在溶液中不能大量共存,故C错误;
D.CO32-、H+之间发生反应,在溶液中不能大量共存,故D错误;
故选A.
B.Ba2+、SO42-之间反应生成硫酸钡,在溶液中不能大量共存,故B错误;
C.Mg2+、H+都与OH-反应,在溶液中不能大量共存,故C错误;
D.CO32-、H+之间发生反应,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,题目难度中等,注意熟练掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等,试题有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
有一在空气中暴露过的KOH固体,经分析知含水7.12%,K2CO32.88%,KOH 90%,若将此样品1g加入到46.00mL 1mol/L盐酸中,过量的酸再用1.07mol/LKOH溶液恰好中和,蒸发中和后的溶液可得固体( )g.
| A、6.07 | B、2.62 |
| C、4.54 | D、3.43 |
已知某氧化剂XO3-中+5价的X能被Na2SO3还原成0价,则还原含有2.4×10-3molXO3-的溶液,需0.2mol?L-1的Na2SO3溶液的体积为( )
| A、40mL | B、30mL |
| C、20mL | D、10mL |
H2和I2在一定条件下能发生反应:H2(g)+I2(g)═2HI(g)△H=-a kJ/mol下列说法正确的是( )
已知:
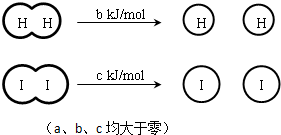
已知:

| A、H2、I2和HI分子中的化学键都是非极性共价键 |
| B、断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ |
| C、相同条件下,1 mol H2(g)和1mol I2(g)总能量小于2 mol HI (g)的总能量 |
| D、向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ |
石油是重要的能源和化工原料,我国南海因为富含石油资源而被菲律宾等邻国觊觎.下列燃料不是从石油中分离出来的是( )
| A、煤油 | B、柴油 | C、酒精 | D、汽油 |
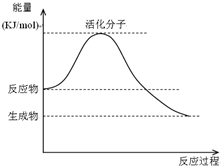 (1)如图是某化学反应中的能量变化图.
(1)如图是某化学反应中的能量变化图.