题目内容
下列说法中正确的是( )
| A、1 mol H2的质量与它的相对分子质量相等 |
| B、NaOH的摩尔质量是40 g?mol-1 |
| C、1 mol H2O的质量为18 g?mol-1 |
| D、氧气的摩尔质量等于它的相对分子质量 |
考点:摩尔质量
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、质量单位为g,相对分子质量单位为1;
B、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量;
C、质量单位为g;
D、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量.
B、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量;
C、质量单位为g;
D、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量.
解答:
解:A、质量单位为g,相对分子质量单位为1,1mol H2的质量数值上与它的相对分子质量相等,故A错误;
B、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量,NaOH的摩尔质量是40 g?mol-1,故B正确;
C、质量单位为g,1 mol H2O的质量为18 g,故C错误;
D、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量,氧气的摩尔质量数值上等于它的相对分子质量,故D错误;
故选B.
B、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量,NaOH的摩尔质量是40 g?mol-1,故B正确;
C、质量单位为g,1 mol H2O的质量为18 g,故C错误;
D、摩尔质量是单位物质的量的物质的质量,单位为g/mol,数值上等于其相对分子质量或相对原子质量,氧气的摩尔质量数值上等于它的相对分子质量,故D错误;
故选B.
点评:本题考查了摩尔质量的概念分析判断,掌握概念实质是解题关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
普通干电池中装有二氧化锰和其他物质,二氧化锰的作用是( )
| A、和正极作用把碳变成CO2 |
| B、把正极附近生成的氢气氧化成水 |
| C、电池中发生化学反应的催化剂 |
| D、和负极作用,将锌变成锌离子Zn2+ |
下列化学用语表达正确的是( )
A、乙酸的分子比例模型图为: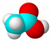 |
B、Mg原子结构示意图: |
| C、次氯酸的结构式为:H-Cl-O |
| D、丙烯的结构简式:CH3CH2CH |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,16g14CH4所含中子数目为8NA |
| B、25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
| C、标准状况下,22.4 LCH4和CH3CH2OH的混合物所含分子数为NA |
| D、含0.2 NA个阴离子的Na2O2和水完全反应转移0.2 mol电子 |
下列反应的离子方程式书写正确的是( )
| A、FeSO4溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+═2Fe3++2H2O | ||||
B、以石墨作电极电解CuCl2溶液:2Cl-+2H2O
| ||||
| C、2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(g)△H=-285.8kJ/mol | ||||
| D、NaHSO4溶液与足量Ba(OH)2溶液混合:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
描述或解释下列现象的离子方程式,不正确的是( )
| A、滴有蓝色石蕊的烧碱溶液里通CO2至颜色变红:CO2+2OH-═CO32-+H2O |
| B、稀醋酸溶解水垢中的碳酸钙:2CH3COOH+CaCO3═Ca2++2CH3COO-+H2O+CO2↑ |
| C、碳酸氢铵溶液中加足量石灰水:NH4++HCO3-+Ca2++2OH-═CaCO3↓+NH3?H2O+H2O |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O═Fe(OH)3↓+3HClO |
用铂电极分别电解下列各盐的水溶液,当消耗相同电量时,在阴极上析出的金属质量最大且溶液pH减小的是( )
| A、CuCl2 |
| B、KCl |
| C、CuSO4 |
| D、Al(NO3)3 |
