题目内容
(反应:aA(g)+bB(g)
cC(g)(△H<0)在等容条件下进行.改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图1所示:
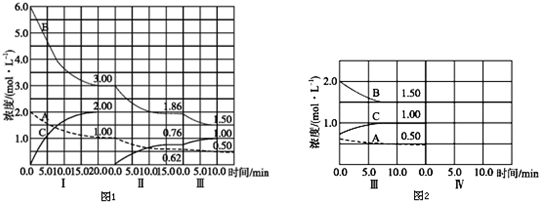
回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为 ;
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的值是 ,
(4)由第一次平衡到第二次平衡,采取的措施是 ;
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2 T3(填“>”“<”或“=”),判断的理由是 ;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在图2中用曲线表示第Ⅳ阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
| 催化剂 |

回答问题:
(1)反应的化学方程式中,a:b:c为
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的值是
(4)由第一次平衡到第二次平衡,采取的措施是
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在图2中用曲线表示第Ⅳ阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
考点:物质的量或浓度随时间的变化曲线,化学平衡的影响因素
专题:化学平衡专题
分析:(1)由图可知第Ⅰ阶段,平衡时△c(A)=2mol/L-1mol/L=1mol/L,△c(B)=6mol/L-3mol/L=3mol/L,△c(C)=2mol/L,根据浓度变化量之比等于化学计量数之比计算;
(2)根据化学反应速率为单位时间浓度的变化值,可计算三个阶段用A表示的化学反应速率,据此判断;
(3)转化率是物质的减少量与初始量的比值,计算三个阶段B的转化率,据此解答;
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动;
(5)第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低;
(6)达到第三次平衡后,将容器的体积扩大一倍,改变条件的瞬间,各组分的浓度变为原来的二分之一,容器体积增大,压强降低平衡向体积增大的方向移动,但增大的物质的量浓度小于第三次平衡时浓度,同时注意各组分物质的量浓度变化量之比等于化学计量数之比,据此作图.
(2)根据化学反应速率为单位时间浓度的变化值,可计算三个阶段用A表示的化学反应速率,据此判断;
(3)转化率是物质的减少量与初始量的比值,计算三个阶段B的转化率,据此解答;
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动;
(5)第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低;
(6)达到第三次平衡后,将容器的体积扩大一倍,改变条件的瞬间,各组分的浓度变为原来的二分之一,容器体积增大,压强降低平衡向体积增大的方向移动,但增大的物质的量浓度小于第三次平衡时浓度,同时注意各组分物质的量浓度变化量之比等于化学计量数之比,据此作图.
解答:
解:(1)由图可知第Ⅰ阶段,平衡时△c(A)=2mol/L-1mol/L=1mol/L,△c(B)=6mol/L-3mol/L=3mol/L,△c(C)=2mol/L,浓度变化量之比等于化学计量数之比,故a:b:c=1mol/L:3mol/L:2mol/L=1:3:2,
故答案为:1:3:2;
(2)vⅠ(A)=
=0.05mol/(L?min),vⅡ(A)=
=0.0253mol/(L?min),
vⅢ(A)=
=0.012mol/(L?min),
故A的平均反应速率vⅠ(A)>vⅡ(A)>vⅢ(A),
故答案为:vⅠ(A)>vⅡ(A)>vⅢ(A);
(3)B的平衡转化率αⅠ(B)=
×100%=50%,αⅡ(B)=
×100%=38%,
αⅢ(B)=
×100%=19%,
B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的值19%;
故答案为:19%;
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动,
故答案为:从反应体系中移出产物C;
(5)第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低,
故答案为:>;此反应为放热反应,降低温度,平衡向正反应方向移动;
(6)(6)达到第三次平衡后,将容器的体积扩大一倍,改变条件的瞬间,各组分的浓度变为原来的二分之一,容器体积增大,压强降低平衡向逆反应方向移动,但增大的物质的量浓度小于第三次平衡时浓度,同时注意各组分物质的量浓度变化量之比等于化学计量数之比,A、B、C的浓度随时间变化的趋势如图: ;
;
故答案为: ;
;
故答案为:1:3:2;
(2)vⅠ(A)=
| 1mol/L |
| 20min |
| 1mol/L-0.62mol/L |
| 15min |
vⅢ(A)=
| 0.62mol/L-0.5mol/L |
| 10min |
故A的平均反应速率vⅠ(A)>vⅡ(A)>vⅢ(A),
故答案为:vⅠ(A)>vⅡ(A)>vⅢ(A);
(3)B的平衡转化率αⅠ(B)=
| 3mol/L |
| 6mol/L |
| 3mol/L-1.86mol/L |
| 3mol/L |
αⅢ(B)=
| 1.86mol/L-1.5mol/L |
| 1.86mol/L |
B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的值19%;
故答案为:19%;
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动,
故答案为:从反应体系中移出产物C;
(5)第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低,
故答案为:>;此反应为放热反应,降低温度,平衡向正反应方向移动;
(6)(6)达到第三次平衡后,将容器的体积扩大一倍,改变条件的瞬间,各组分的浓度变为原来的二分之一,容器体积增大,压强降低平衡向逆反应方向移动,但增大的物质的量浓度小于第三次平衡时浓度,同时注意各组分物质的量浓度变化量之比等于化学计量数之比,A、B、C的浓度随时间变化的趋势如图:
 ;
;故答案为:
 ;
;
点评:本题考查化学反应速率与化学平衡图象、化学平衡有关计算、化学反应速率、化学平衡影响因素等,注意合理分析题中信息数据,本题难度中等

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
NO和CO都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化碳气体:2NO+2CO=N2+2CO2对此反应,下列叙述正确的是( )
| A、使用催化剂能加快反应速率 |
| B、改变压强对反应速率没有影响 |
| C、冬天气温低,反应速率降低,对人体危害更大 |
| D、无论外界条件怎样改变,均对此化学反应的速率无影响 |
 下列各组物质不能按如图所示(表示反应一步完成)关系转化的是( )
下列各组物质不能按如图所示(表示反应一步完成)关系转化的是( )| 选项 | a | b | c |
| A | SiO2 | Na2SiO3 | H2SiO3 |
| B | Fe2O3 | FeCl3 | Fe(OH)3 |
| C | Al | Al(OH)3 | Al2O3 |
| D | NaHCO3 | Na2CO3 | NaOH |
| A、A | B、B | C、C | D、D |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1.0L1.0 mol?L-1的Na[Al(OH)4]水溶液中含有的氧原子数为2NA |
| B、常温常压下,8gO2含有4nA个电子 |
| C、标准状况下,22.4L盐酸含有nA个HCl分子 |
| D、1molNa被完全氧化生成Na2O2,失去2nA个电子 |
镍(Ni)镉(Cd)可充电的电池,放电时,电极材料是Cd和NiO(OH),电解质是KOH,电极反应分别是:
Cd+2OH--2e-=Cd(OH)2;2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-.下列说法不正确的是( )
Cd+2OH--2e-=Cd(OH)2;2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-.下列说法不正确的是( )
| A、电池放电时,负极周围溶液的pH不断减小 |
| B、电池放电时总反应是Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2 |
| C、电池充电时,镉(Cd)元素被氧化 |
| D、电池充电时,电池的正极和电源的正极相连接 |
 某化学研究性学习小组探究Fe3+和SO32-之间发生的反应.
某化学研究性学习小组探究Fe3+和SO32-之间发生的反应.