题目内容
10.(1)根据官能团对下列有机物进行分类,将它们的类别填写在横线上.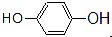 酚
酚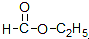 酯
酯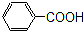 羧酸
羧酸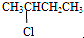 氯代烃
氯代烃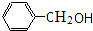 醇CH3C≡CH炔.
醇CH3C≡CH炔.
分析 酚类含有羟基,且羟基与苯环直接相连;
含有-COO-的属于酯类;
含有-COOH的属于羧酸;
烃中的H原子被卤素原子取代得打的产物是卤代烃;
醇类含有羟基,且羟基不与苯环直接相连;
含有碳碳三键的是炔烃.
解答 解: 含有羟基,且羟基直接与苯环相连,属于酚;
含有羟基,且羟基直接与苯环相连,属于酚;
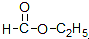 含有-COO-,属于酯类;
含有-COO-,属于酯类;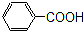 含有-COOH,属于羧酸;
含有-COOH,属于羧酸;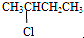 含有-Cl,属于卤代烃;
含有-Cl,属于卤代烃;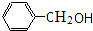 含有羟基,且羟基不与苯环相连,属于醇;
含有羟基,且羟基不与苯环相连,属于醇;
CH3C≡CH含有碳碳三键,属于炔烃,故答案为:酚;酯;羧酸;氯代烃;醇;炔.
点评 本题主要考查的是有机物的结构以及其分类,掌握各种物质的官能团是解决本题的关键,难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
18.下列关于官能团的说法,正确的是( )
| A. | 苯及其同系物没有官能团 | B. | 卤代烃没有官能团 | ||
| C. | 醛的官能团为羰基 | D. | 羧酸和酯的官能团相同 |
5.关于重结晶的说法,错误的是( )
| A. | 被重结晶提纯的物质的溶解度随温度变化大 | |
| B. | 溶解度很小的杂质留在了热滤的滤渣里 | |
| C. | 重结晶的步骤为:加热溶解、冷却过滤、结晶 | |
| D. | 重结晶的首要工作是选择适当的溶剂 |
15.下列由实验现象得出的结论正确的是( )
| A. | 向某无色液中加BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有Ag+ | |
| B. | 向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32- | |
| C. | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH4Cl固体可以升华 | |
| D. | 向NaBr溶液中滴入少量氯水和CCl4,振荡、静置,溶液下层呈橙红色,说明Br-还原性强于Cl- |
2.99℃时,Kw=1.0×10-12,该温度下测得0.1mol/LNa2A溶液的pH=6.下列说法不正确的是( )
| A. | H2A在水溶液中的电离方程式为H2A=2H++A2- | |
| B. | 该温度下,将0.01mol/L的H2A溶液稀释20倍后溶液的pH=3 | |
| C. | 体积相同,pH均为1的盐酸和H2A溶液分别与足量的Zn反应,产生H2较多的是H2A | |
| D. | 将0.1mol/L的H2A溶液与0.2mol/L的氨水等体积混合后,溶液中浓度最大的离子是NH4+ |
20.下列涉及的实验方案或工业方案不能达到目的是( )
| A. | 用FeCl3溶液刻制铜材电路板 | |
| B. | 用乙醇作萃取剂从碘水中提取碘 | |
| C. | 在常温下用铝制容器贮运浓硫酸 | |
| D. | 向含硫高的煤中加入生石灰,可减少燃料对大气的污染 |