题目内容
5.下列离子方程式正确的是( )| A. | 氯气与氢氧化钠溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 碳酸钙加入盐酸中:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁与FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 向MgCl2溶液加入氨水:Mg2++2OH-═Mg(OH)2↓ |
分析 A.氯气与氢氧化钠溶液反应生成NaCl、NaClO和水;
B.碳酸钙不溶于水,应写成化学式;
C.电荷不守恒;
D.一水合氨为弱电解质,应写成化学式.
解答 解:A.氯气与氢氧化钠溶液反应生成NaCl、NaClO和水,离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,故A正确;
B.碳酸钙不溶于水,应写成化学式,离子方程式为CaCO3+2H+═Ca2++H2O+CO2↑,故B错误;
C.电荷不守恒,应为Fe+2Fe3+═3Fe2+,故C错误;
D.一水合氨为弱电解质,应写成化学式,离子方程式为Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+,故D错误.
故选A.
点评 本题考查离子方程式的书写,为高考常见题型,注意把握常见离子的性质以及离子方程式的书写方法,答题时从守恒的角度和粒子符号的角度分析,难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
15.短周期主族元素W、X、Y、Z的原子序数依次增大.元素W的原子内层电子数是最外层电子数的2倍,元素X的单质是电池常用的惰性电极材料,元素Y的原子最外层电子数等于电子层数,元素Z的原子最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 化合物XZ2中,各原子均满足8电子的稳定结构 | |
| B. | 元素X与氢元素能形成原子数目之比为1:1的化合物 | |
| C. | Y的单质与稀硫酸、浓硫酸均可发生氧化还原反应 | |
| D. | Z的单质在加热条件下会与Fe反应生成Fe3Z4 |
16.在可逆反应mX+nY?pZ+qW中,在反应开始后的10s,若用每种物质的浓度增加表示该段时间的平均反应速率时分别为v(X=0.5amol•L-1•s-1,v(Y)=0.25amol•L-1•s-1,v(Z)=amol•L-1•s-1,v(W)=1.5amol•L-1•s-1.若用每种物质的浓度减少表示该段时间的平均反应速率时分别为v(X)=amol•L-1•s-1,v(Y)=0.5amol•L-1•s-1,v(Z)=0.5amol•L-1•s-1,v(W)=0.75amol•L-1•s-1,则m:n:p:q为( )
| A. | 2:1:2:3 | B. | 2:1:4:6 | C. | 2:1:4:3 | D. | 1:1:1:1 |
13.一定温度下,在3个体积均为1.0L的容量密闭容器中反应2H2(g)+CO(g)?CH3OH(g) 达到平衡,下列说法正确的是( )
| 容器 | 温度/℃ | 物质的起始浓度/mol•L-1 | 物质的平衡浓度/mol•L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | 该方应的正反应放热 | |
| B. | 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 | |
| C. | 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍 | |
| D. | 达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大 |
20.关于由铜、锌和稀硫酸组成的原电池中,下列各叙述正确的是( )
| A. | 负极附近c(Zn2+)减小 | |
| B. | 溶液的pH变小 | |
| C. | H+向负极移动 | |
| D. | 若Cu,Zn两极上同时有气泡逸出,则说明Zn片不纯 |
10.下列物质的除杂方案正确的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | Cl2 (g) | HCl(g) | 饱和NaCl溶液、浓硫酸 | 洗气 |
| B | Na2CO3(aq) | NaHCO3(aq) | 过量NaOH溶液 | 洗液 |
| C | 铁粉(s) | 铝粉(s) | 过量NaOH溶液 | 过滤 |
| D | FeCl3(aq) | AlCl3(aq) | 过量氨水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.下列化工生产过程中,未涉及氧化还原反应的是( )
| A. | 海带提碘 | B. | 氯碱工业 | C. | 氨碱法制碱 | D. | 海水提溴 |
8.下列化学用语的表达正确的是( )
| A. | 原子核内有10个中子的氧原子:${\;}_{6}^{18}$O | |
| B. | 氯原子的结构示意图: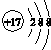 | |
| C. | Fe3+的最外层电子排布式为3s23p63d5 | |
| D. | 基态铜原子的外围电子排布图: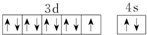 |
9.在电解质溶液中插入M、N电极,并连接直流电源进行电解,可以看到两极上均有气泡产生,电解后测定电解质溶液,其H+浓度无变化.符合这些条件的是( )
| A. | 两个电极均为铁片,M是阴极,电解质溶液是0.4%的NaOH溶液 | |
| B. | 两个电极均为石墨,M是阳极,电解质溶液是0.4%的H2SO4溶液 | |
| C. | M是铁片,作阴极,N是石墨,电解质溶液是0.4%的Ba(NO3)2溶液 | |
| D. | M是铁片,作阴极,N是石墨,电解质溶液是0.4%的HCl溶液 |