题目内容
4.下列电离的方程式,正确的是( )| A. | CH3COOH═CH3COO-+H+ | B. | NaOH═Na++OH- | ||
| C. | H2SO4═H++SO42- | D. | KClO3═K++Cl-+3O2- |
分析 A.醋酸是弱酸,部分电离;
B.NaOH是强电解质,在溶液中完全电离;
C.硫酸是二元酸强酸,在溶液中完全电离出2个氢离子;
D.氯酸钾在溶液中电离出钾离子和氯酸根离子.
解答 解:A.醋酸是弱酸,部分电离,应该用可逆号表示,则电离方程式为:CH3COOH?CH3COO-+H+,故A错误;
B.NaOH是强电解质,在溶液中完全电离,则电离方程式为:NaOH═Na++OH-,故B正确;
C.硫酸是二元酸强酸,在溶液中完全电离出2个氢离子,则电离方程式为:H2SO4═2H++SO42-,故C错误;
D.氯酸钾在溶液中电离出钾离子和氯酸根离子,则电离方程式为:KClO3═K++ClO3-,故D错误.
故选B.
点评 本题考查了电离方程式的书写,题目难度不大,注意把握强弱电解的判断和电离方程式的书写,侧重于基础知识的考查.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
14.短周期主族元素X、Y、Z、W原子序数依次增大,X元素的单质可在自然界中形成最硬的矿石,Y原子最外层有6个电子,Z元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,W与X同主族.下列叙述正确的是( )
| A. | 原子最外层电子数由少到多的顺序:X=W<Y<Z | |
| B. | 原子半径由大到小的顺序:r(W)>r(X)>r(Y)>r(Z) | |
| C. | 元素非金属性由强到弱的顺序:X、Y、W | |
| D. | 元素的简单气态氢化物的稳定性由强到弱的顺序:Y、X、W |
12.下列操作不能达到目的是( )
| 选项 | 目的 | 操作 |
| A | 配置100mL 1.0mol•L-1CuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| B | 除去KNO3固体中少量NaCl | 将混合物制成熟的饱和溶液,冷却结晶,过滤 |
| C | 提取溴水中的Br2 | 向溶液中加入乙醇后振荡,静置,分液 |
| D | 检验溶液中是否含有NH4+ | 取少量溶液于试管中,加入NaOH后,加热,在试管口放置 一块湿润的红色石蕊试纸 |
| A. | A | B. | B | C. | C | D. | D |
19.2015年温州马拉松参赛选手需佩戴含硅的感应芯片计时.硅的元素符号是( )
| A. | Mg | B. | Si | C. | S | D. | Fe |
9.下列化学用语表述正确的是( )
| A. | 溴单质:Br | B. | 氯离子的结构示意图: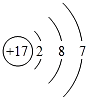 | ||
| C. | H2O的结构式: | D. | CaCl2的电子式: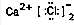 |
16.下列有关SO2的说法不正确的是( )
| A. | 把SO2通入紫色石蕊溶液中,石蕊溶液 会变红 | |
| B. | 把SO2通入品红溶液中,品红溶液会褪色 | |
| C. | 将足量SO2通入酸性高锰酸钾溶液中,溶液褪色 | |
| D. | 把SO2通入氯化钡溶液中,溶液会出现白色沉淀 |
13.下列反应属于取代反应的是( )
| A. | 乙醇在浓硫酸作用下加热制乙烯 | B. | 石油裂解制丙烯 | ||
| C. | 苯和液溴反应制溴苯 | D. | 乙烯制聚乙烯 |
14.下列说法能用平衡移动原理解释的是( )
| A. | 在电解水实验中,加入硫酸钠可以提高电解效率 | |
| B. | 碳酸氢钠溶液与硫酸铝溶液混合有沉淀和气体生成 | |
| C. | 铁制品在海水中比在纯水中更易腐蚀 | |
| D. | 在双氧水中加FeCl3溶液可使产生O2速率加快 |
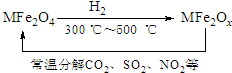 新型纳米材料氧缺位铁酸盐MFe2Ox(3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温与H2反应制得.常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图:
新型纳米材料氧缺位铁酸盐MFe2Ox(3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温与H2反应制得.常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图: