题目内容
17.用双线桥标出电子转移的方向和数目(1)2Na+Cl2═2NaCl
(2)2H2S+SO2═3S↓+2H2O.
分析 (1)Na元素的化合价升高,Cl元素的化合价降低,该反应转移2e-;
(2)硫化氢中硫元素的化合价变化由-2价变为0价,二氧化硫中硫元素的化合价由+4价变为0价,该反应转移4e-.
解答 解:(1)Na元素化合价由0价变为+1价、Cl元素化合价由0价变为-1价,转移电子数为2e-,转移电子方向和数目为 ,
,
故答案为: ;
;
(2)该反应中,硫化氢中硫元素的化合价变化由-2价变为0价,二氧化硫中硫元素的化合价变化为:由+4价变为0价,所以得失电子最小公倍数是4,则该反应中转移电子方向和数目为: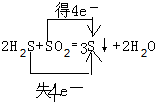 ,故答案为:
,故答案为: .
.
点评 本题考查氧化还原反应,为高频考点,把握元素的化合价变化及转化电子表示方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.在化学反应 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+3H2 中,H2O的作用是( )
| A. | 还原剂 | B. | 氧化剂 | C. | 催化剂 | D. | 溶剂 |
2.将含Mg的两种金属混合物30克与足量稀盐酸反应产生标况下11.2L(标准状况下),则混合物中另一金属可能为( )
| A. | Al | B. | Na | C. | Cu | D. | Fe |
9.无色透明溶液中,下列各组离子能大量共存的是( )
| A. | HCO3-、ClO-、K+、H+ | B. | Na+、Fe2+、NO3-、H+ | ||
| C. | K+、Mg2+、Cl-、SO42- | D. | OH-、NH4+、Cl-、SO32- |
7.对下列气体进行“喷泉”实验,在干燥的烧瓶中分别装入下列气体,打开止水夹,形成喷泉,其中溶液不能充满烧瓶的是( )
| A. | NH3 | B. | NO2 | ||
| C. | HCl | D. | 体积比为4:1的NO2和O2的混合气体 |

 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基. ,反应类型:氧化反应.
,反应类型:氧化反应. ,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.
,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.