题目内容
4.室温下某溶液中由水电离出的H+浓度为1.0×10-13 mol•L-1,则在此溶液中一定不可能大量存在的离子组是( )| A. | Al3+、K+、NO3-、Cl- | B. | K+、Na+、HS-、Cl- | ||
| C. | Na+、AlO2-、SO42-、NO3- | D. | Ba2+、Na+、Cl-、NO3- |
分析 由水电离出的H+浓度为1.0×10-13 mol•L-1,该溶液中存在大量氢离子或氢氧根离子,
A.四种离子之间不反应,都不与氢离子反应;
B.硫氢根离子与氢离子、氢氧根离子反应;
C.四种离子之间不反应,都不与氢氧根离子反应;
D.四种离子之间不反应,都不与氢离子、氢氧根离子反应.
解答 解:室温下某溶液中由水电离出的H+浓度为1.0×10-13 mol•L-1,该溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,
A.Al3+、K+、NO3-、Cl-之间不发生反应,都不与氢离子反应,在酸性溶液中能够大量共存,故A错误;
B.HS-与氢离子和氢氧根离子反应,在溶液中一定不能大量共存,故B正确;
C.Na+、AlO2-、SO42-、NO3-之间不反应,都不与氢氧根离子反应,在碱性溶液中能够大量共存,故C错误;
D.Ba2+、Na+、Cl-、NO3-之间不反应,都不与氢离子、氢氧根离子反应,在溶液中一定能够大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
15.下列可以使有色布条褪色的物质是( )
| A. | 久置的氯水 | B. | 次氯酸钠溶液 | C. | 漂白粉溶液 | D. | 氯化钙溶液 |
16.下图是CH4、CCl4、CH3Cl的分子球棍模型图,下列说法正确的是( )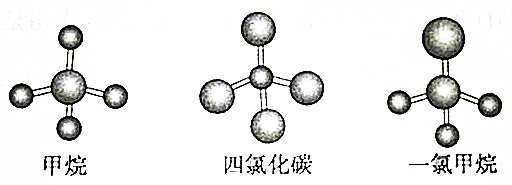

| A. | CH4、CCl4和CH3Cl都是正四面体结构 | |
| B. | CH4、CCl4都是正四面体结构 | |
| C. | CH4和CCl4中的化学键均为非极性键 | |
| D. | CH4、CCl4的结构相同,性质也相同 |
4.某二元甘油酯可以看成是甘油(丙三醇)与一元羧酸反应的产物,符合条件的甘油酯共有15种,则一元羧酸最少有( )
| A. | 五种 | B. | 两种 | C. | 三种 | D. | 四种 |
5.以下自发进行反应可用能量判据来解释的是( )
| A. | 硝酸铵自发地溶于水 | |
| B. | 2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ•mol-1 | |
| C. | (NH4 )2 CO3(s)═NH4HCO3(s)+NH3(g);△H=+74.9 kJ/mol | |
| D. | 2H2(g)+O2(g)═2H2O(l);△H=-571.6 KJ/mol |
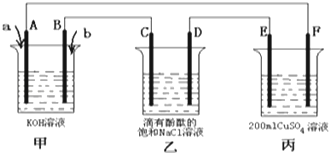
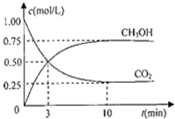 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,