题目内容
5.反应N2(g)+3H2(g)?2NH3(g)△H<0;若升温,则反应速率v(正)、v(逆)的变化是( )| A. | 同时减少 | B. | 同时增大 | C. | v(正)增大,v(逆)减少 | D. | v(正)减少,v(逆)增大 |
分析 化学反应无论是吸热反应还是放热反应,温度升高,化学反应速率都增大.
解答 解:化学反应无论是吸热反应还是放热反应,温度升高,活化分子的百分含量增大,有效碰撞的次数增大,化学反应速率都增大.
故选B.
点评 本题考查温度对化学反应速率的影响,题目难度不大,注意温度对反应速率的影响与反应的吸、放热无关.

练习册系列答案
相关题目
15.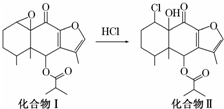 我国科研人员以蹄叶囊青为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
我国科研人员以蹄叶囊青为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
 我国科研人员以蹄叶囊青为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
我国科研人员以蹄叶囊青为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )| A. | 化合物Ⅰ能使酸性KMnO4溶液褪色 | |
| B. | 化合物Ⅰ分子中含有6个手性碳原子 | |
| C. | 化合物Ⅱ一定条件下能发生取代、消去及加成反应 | |
| D. | 检验化合物Ⅱ中是否含化合物Ⅰ可用Br2的CCl4溶液 |
16.下列离子可以大量共存的是( )
| A. | Mg2+ Na+ SO42- OH- | B. | Ca2+K+ HCO3-OH- | ||
| C. | Na+ H+ CH3COO- SO42- | D. | Ba2+ K+NO3-Cl- |
13.下列物质不能用单质直接化合而成的是( )
| A. | FeS | B. | SO3 | C. | FeCl3? | D. | HgS |
10.下列反应过程能量变化如下所示:
H2(g)+Cl2(g)═2HCl(g)△H
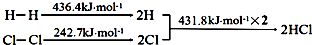
下列说法错误的是( )
H2(g)+Cl2(g)═2HCl(g)△H
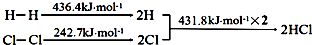
下列说法错误的是( )
| A. | H-H键比Cl-Cl键稳定 | |
| B. | △H=-184.5 kJ•mol-1 | |
| C. | 正反应活化能比逆反应活化能高 | |
| D. | 在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时△H相同 |
17.常温下,下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.有关上述溶液的比较中,正确的是( )
| A. | 将等体积的①、②溶液混合后,盐酸会抑制醋酸的电离,所以pH>2 | |
| B. | 将一定体积的②、③溶液混合后,溶液显碱性,则该混合溶液中c(Cl-)>c(NH4+) | |
| C. | 将一定体积的①、④溶液混合后,溶液显酸性,则V(NaOH)可能等于V(CH3COOH) | |
| D. | 向等体积的③、④溶液中加水稀释10倍,稀释后溶液中由水电离的c(H+):③>④ |
14.设NA表示阿伏伽德罗常数的值,下列叙述中不正确的是( )
| A. | 室温下,46gNO2和N2O4的混合气体中含有NA个氮原子 | |
| B. | 1mol12C18O2中所含的中子数为26NA | |
| C. | 常温下,1L0.1mol/LCH3COONa溶液中含有CH3COO-和Na+总数为0.2NA | |
| D. | 常温下,1LpH=12的氨水中含有OH-的数目为0.01NA |
