题目内容
17.下列离子方程式改写成化学方程式,正确的是( )| A. | Cu2++2OH-→Cu(OH)2↓ 3CuSO4+2Fe(OH)3→Fe2(SO4)3+3Cu(OH)2↓ | |
| B. | S2-+2Ag+→Ag2S↓ H2S+2AgNO3→Ag2S↓+2HNO3 | |
| C. | CO32-+2H+→H2O+CO2↑ Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑ | |
| D. | Ag++Cl-=AgCl↓ AgNO3+NaCl=NaNO3+AgCl↓ |
分析 A.CuSO4与Fe(OH)3不反应;
B.H2S在离子反应中保留化学式,且Ag2S、HNO3可发生氧化还原反应;
C.CH3COOH在离子反应中保留化学式;
D.AgNO3+NaCl=NaNO3+AgCl↓的离子反应为Ag++Cl-=AgCl↓.
解答 解:A.CuSO4与Fe(OH)3不反应,Cu2++2OH-=Cu(OH)2↓表示可溶性铜盐与强碱反应生成氢氧化铜和可溶性盐的反应,故A不选;
B.H2S在离子反应中保留化学式,且Ag2S、HNO3可发生氧化还原反应,则S2-+2Ag+=Ag2S↓表示可溶性硫化物的盐类物质与硝酸银反应,故B不选;
C.CH3COOH在离子反应中保留化学式,则CO32-+2H+=H2O+CO2↑表示可溶性碳酸盐与强酸反应,故C不选;
D.AgNO3+NaCl=NaNO3+AgCl↓的离子反应为Ag++Cl-=AgCl↓,故D选;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握离子反应的书写方法及意义为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
7.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 14g乙烯、丙烯、丁烯的混合气体中所含原子数为3NA | |
| B. | 28g乙烯所含共用电子对数目为5NA | |
| C. | 标准状况下,11.2 L氯仿所含分子数为0.5 NA | |
| D. | 46g乙醇中含有C-H键数目为6NA |
8.钴及其合金在电机、机械、化工、航空和航天等工业部门得到广泛的应用,并成为一种重要的战略金属.
Ⅰ.钴酸锂电池的正极采用钴酸锂LiCoO2,负极采用金属锂和碳的复合材料,该电池的反应为:LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6,写出放电时负极的电极反应LixC6-xe-=6C+xLi+.
Ⅱ.碱式碳酸钴[Cox(OH)y(CO3)z]常用做电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物.为了确定其组成,某化学兴趣小组同学设计了如图(甲、乙、丙)所示的装置进行实验.

实验步骤如下:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,检查装置气密性;
③加热玻璃管,当乙装置中不再有气泡产生,停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算.
(1)从下列图示(A-D)选出合理的装置填入方框中,使整套实验装置完整(选填字母序号,可重复选用):
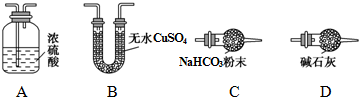
甲D;乙A;丙D.
甲装置的作用是吸收空气中的H2O和CO2,减少实验误差.
(2)补充完整步骤③不再有气泡产生;步骤④中缓缓通入空气数分钟的目的是将生成的CO2和H2O全部赶入乙和丙吸收.
(3)若按正确装置进行实验,测得如下数据:
则该碱式碳酸钴的化学式为Co3(OH)4(CO3)2.
(4)为了比较亚硫酸和碳酸的酸性强弱,某同学用如下(A、B)装置进行实验:

①试剂A是酸性高锰酸钾溶液,试剂B是澄清石灰水.
②若将SO2通入水中至饱和,请设计实验证明亚硫酸是弱酸:首先测得亚硫酸饱和溶液的pH,然后取一定体积的饱和溶液稀释10倍再测pH,若pH差小于1,说明亚硫酸是弱酸用中和滴定法,根据氢氧化钠溶液的体积可知溶液中亚硫酸的浓度,比较亚硫酸的浓度和氢离子的浓度,若亚硫酸的浓度大于氢离子的浓度,则亚硫酸为弱酸.
Ⅰ.钴酸锂电池的正极采用钴酸锂LiCoO2,负极采用金属锂和碳的复合材料,该电池的反应为:LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6,写出放电时负极的电极反应LixC6-xe-=6C+xLi+.
Ⅱ.碱式碳酸钴[Cox(OH)y(CO3)z]常用做电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物.为了确定其组成,某化学兴趣小组同学设计了如图(甲、乙、丙)所示的装置进行实验.

实验步骤如下:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,检查装置气密性;
③加热玻璃管,当乙装置中不再有气泡产生,停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算.
(1)从下列图示(A-D)选出合理的装置填入方框中,使整套实验装置完整(选填字母序号,可重复选用):

甲D;乙A;丙D.
甲装置的作用是吸收空气中的H2O和CO2,减少实验误差.
(2)补充完整步骤③不再有气泡产生;步骤④中缓缓通入空气数分钟的目的是将生成的CO2和H2O全部赶入乙和丙吸收.
(3)若按正确装置进行实验,测得如下数据:
| 乙装置的质量(g) | 丙装置的质量(g) | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |
(4)为了比较亚硫酸和碳酸的酸性强弱,某同学用如下(A、B)装置进行实验:

①试剂A是酸性高锰酸钾溶液,试剂B是澄清石灰水.
②若将SO2通入水中至饱和,请设计实验证明亚硫酸是弱酸:首先测得亚硫酸饱和溶液的pH,然后取一定体积的饱和溶液稀释10倍再测pH,若pH差小于1,说明亚硫酸是弱酸用中和滴定法,根据氢氧化钠溶液的体积可知溶液中亚硫酸的浓度,比较亚硫酸的浓度和氢离子的浓度,若亚硫酸的浓度大于氢离子的浓度,则亚硫酸为弱酸.
5.A-F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如表所示:
请回答下列问题:
(1)A在元素周期表中的位置是第三周期第ⅡA族;A与E形成的化合物的电子式是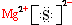 .
.
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是2Fe3++Cu═2Fe2++Cu2+.
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(4)F的氢氧化物的是两性(填“酸性”“碱性”“两性”)氢氧化物,其电离方程式是Al3++3OH-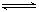 Al(OH)3
Al(OH)3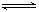 H++AlO2-+H2O;F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
H++AlO2-+H2O;F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 元素 | 结构或性质 |
| A | 原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
(1)A在元素周期表中的位置是第三周期第ⅡA族;A与E形成的化合物的电子式是
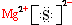 .
.(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是2Fe3++Cu═2Fe2++Cu2+.
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(4)F的氢氧化物的是两性(填“酸性”“碱性”“两性”)氢氧化物,其电离方程式是Al3++3OH-
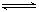 Al(OH)3
Al(OH)3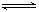 H++AlO2-+H2O;F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
H++AlO2-+H2O;F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
12.下列各组中的两种物质互为同分异构体的是( )
| A. | 乙烷和乙酸 | B. | 淀粉和纤维素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙醇和二甲醚 |
2.等体积、物质的量浓度之比为6:2:3的AClx、BCly、CClz三种盐溶液分别与足量AgNO3溶液反应,生成等量沉淀,则x:y:z为( )
| A. | 1:2:3 | B. | 1:3:2 | C. | 2:4:5 | D. | 2:3:1 |
6.下表列出了A~R 9种元素在周期表中的位置:
(1)F元素的名称为氧;画出B的原子结构示意图: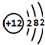 .
.
(2)这9种元素中,化学性质最不活泼的是Ar;既具有非金属元素的某些性质,又可能具有金属元素的某些性质的元素是B、Si.(填元素符号)
(3)A、D、E三种元素的最高价氧化物形成的晶体中属于分子晶体的是CO2,A、B两元素的氧化物中熔点较高的是MgO,C、D、F形成的氢化物分子中共价键的极性由强到弱的顺序为H2O>CH4>BH3(或B2H6).(填化学式)
(4)工业上用D的一种单质为原料生产E单质粗品的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si.
(5)G和H的原子序数相差18.(填数字)
(6)写出一个能证明G比H活泼的化学方程式Cl2+2KBr=2KCl+Br2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | C | D | F | |||||
| 三 | B | E | G | R | ||||
| 四 | A | H |
 .
.(2)这9种元素中,化学性质最不活泼的是Ar;既具有非金属元素的某些性质,又可能具有金属元素的某些性质的元素是B、Si.(填元素符号)
(3)A、D、E三种元素的最高价氧化物形成的晶体中属于分子晶体的是CO2,A、B两元素的氧化物中熔点较高的是MgO,C、D、F形成的氢化物分子中共价键的极性由强到弱的顺序为H2O>CH4>BH3(或B2H6).(填化学式)
(4)工业上用D的一种单质为原料生产E单质粗品的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si.
(5)G和H的原子序数相差18.(填数字)
(6)写出一个能证明G比H活泼的化学方程式Cl2+2KBr=2KCl+Br2.
7.用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示.下列说法正确的是( )
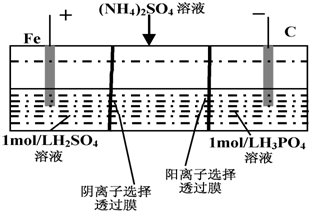

| A. | 阳极室溶液由无色变成棕黄色 | |
| B. | 阴极的电极反应式为:4OH--4e-=2H2O+O2↑ | |
| C. | 电解一段时间后,阴极室溶液中的酸性减弱 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
 .其反应类型为消去反应.检验生成的乙烯要将气体先后通入氢氧化钠溶液、酸性高锰酸钾溶液或溴水中.(填试剂名称)
.其反应类型为消去反应.检验生成的乙烯要将气体先后通入氢氧化钠溶液、酸性高锰酸钾溶液或溴水中.(填试剂名称)