题目内容
16.下列有关反应热的说法正确的是( )| A. | 吸热反应一定需要加热,放热反应一定不需要加热 | |
| B. | 甲烷的燃烧热△H=-890kJ/mol,则甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890kJ/mol | |
| C. | 常温常压下:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ/mol则有:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H=-114.6 kJ/mol | |
| D. | S (s)+O2(g)=SO2(g)△H1=-Q1 kJ/mol S (g)+O2(g)=SO2(g)△H2=-Q2 kJ/mol,则Q1<Q2 |
分析 A、吸热反应不一定需要加热,放热反应不一定不需要加热;
B、燃烧热是生成稳定的氧化物;
C、根据SO42-、Ba2+反应生成BaSO4,需要放出热量来判断;
D、固体硫转化为气态硫要吸热.
解答 解:A、吸热反应不一定需要加热,如氢氧化钡晶体与氯化铵晶体搅拌即可发生反应,不需要加热,碳燃烧要在点燃的条件下才能发生,故A错误;
B、燃烧热是生成稳定的氧化物,水是生成液态水,故B错误;
C、因SO42-、Ba2+反应生成BaSO4,需要放出热量,所以反应热小于-114.6 kJ•mol-1,故C错误;
D、固体硫转化为气态硫要吸热,所以①S (s)+O2(g)=SO2(g)△H1=-Q1 kJ/mol,②S (g)+O2(g)=SO2(g)△H2=-Q2 kJ/mol,根据盖斯定律,①-②得Q2-Q1>0,则Q1<Q2,故D正确;
故选D.
点评 本题考查热化学方程式以及反应热的计算,题目难度中等,注意理解中和热的概念、把握热化学方程式的书写方法,以及利用化学方程式计算反应热等问题.

练习册系列答案
相关题目
6.已知20°C时AgBr的溶解度为8.4×10-6AgCI的溶解度为1.5×10-4将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银,发生的反应为( )
| A. | 只有AgBr沉淀生成 | B. | AgCl沉淀多于AgBr沉淀 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | AgCl和AgBr沉淀等量生成 |
7.下列离子方程式中正确的是( )
| A. | 碳酸氢铵溶液加足量氢氧化钠并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$H2O+NH3↑ | |
| B. | Na218O2加入H2O中:2Na218O2+2H2O═4Na++4OH-+18O2↑ | |
| C. | 硫酸镁溶液加氨水:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ | |
| D. | 氧化亚铁溶于稀硝酸:FeO+2H+═Fe2++H2O |
4.已知金属钠和水反应的化学方程式为:2Na+2H2O═2NaOH+H2↑.将9.2g金属钠投入到足量的重水D2O中,则产生的气体中含有( )
| A. | 0.2 mol中子 | B. | 0.4 mol电子 | C. | 0.2 mol质子 | D. | 0.4 mol分子 |
11.下列反应的离子方程式错误的是( )
| A. | 大理石溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 在氯化铝溶液中滴加过量的氨水:Al3++3NH3•H2O═Al (OH)3↓+3NH4+ | |
| C. | 硫氢化钠水解:HS-+H2O?H2S+OH- | |
| D. | Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+═2Fe3++2H2O |
1.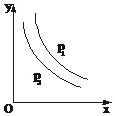 反应:L(s)+aG(g)?bR(g)达到平衡,温度和压强对该反应的影响如图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡,温度和压强对该反应的影响如图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )
 反应:L(s)+aG(g)?bR(g)达到平衡,温度和压强对该反应的影响如图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡,温度和压强对该反应的影响如图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )| A. | 上述反应是放热反应 | B. | a>b | ||
| C. | 上述反应是吸热反应 | D. | 无法确定a、b的大小 |
8.下列能正确表示乙烯结构简式的是( )
| A. | C2H4 | B. | CH2 CH2 | C. | CH2--CH2 | D. | CH2=CH2 |
5.目前银川一中部分学生喜欢使用胶带,四氟乙烯(C2F4)是制作胶带胶黏剂的一种原料.
下面是关于四氟乙烯的几种说法:
①它是由碳、氟两种元素组成的化合物,
②它是由氟气(分子式为:F2)和碳组成的化合物
③它的分子中碳、氟两种元素的原子物质的量比为1:2
这些说法中正确的是( )
下面是关于四氟乙烯的几种说法:
①它是由碳、氟两种元素组成的化合物,
②它是由氟气(分子式为:F2)和碳组成的化合物
③它的分子中碳、氟两种元素的原子物质的量比为1:2
这些说法中正确的是( )
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
6.现有三组溶液,①碘水中提取单质碘 ②碘和四氯化碳的混合物 ③汽油和氯化钠溶液,分离以上混合物的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |