题目内容
5.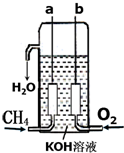 氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制.常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等.已知甲烷燃料电池的负极有碳酸根离子生成,请写出如图所构成的甲烷燃料电池中:a极的电极反应式:CH4+10OH--8e-=CO32-+7H2O,b极的电极反应式:O2+2H2O+4e-=4OH-,若将KOH溶液换为稀H2SO4,则a极的电极反应式:CH4+2H2O-8e-=CO2+8H+.
氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制.常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等.已知甲烷燃料电池的负极有碳酸根离子生成,请写出如图所构成的甲烷燃料电池中:a极的电极反应式:CH4+10OH--8e-=CO32-+7H2O,b极的电极反应式:O2+2H2O+4e-=4OH-,若将KOH溶液换为稀H2SO4,则a极的电极反应式:CH4+2H2O-8e-=CO2+8H+.
分析 甲烷燃料碱性电池中,通入甲烷的电极是负极,负极上甲烷失电子发生氧化反应生成碳酸根离子,正极上氧气得电子发生还原反应;酸性条件下,甲烷在负极上失电子生成二氧化碳,据此分析解答.
解答 解:甲烷燃料碱性电池中,通入甲烷的电极是负极,即a为负极,负极上甲烷失电子发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O;b为正极,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-;若将KOH溶液换为稀H2SO4,甲烷在负极上失电子生成二氧化碳,a极的电极反应式:CH4+2H2O-8e-=CO2+8H+;
故答案为:CH4+10OH--8e-=CO32-+7H2O;O2+2H2O+4e-=4OH-;CH4+2H2O-8e-=CO2+8H+.
点评 本题考查电池反应式及电极反应式的书写,明确正负极上发生的反应及反应产物是解本题关键,注意结合电解质溶液酸碱性书写,题目难度中等.

练习册系列答案
相关题目
16.下列关于化学反应速率和化学平衡的说法正确的是( )
| A. | 对于某一反应来说,化学反应速率始终相同 | |
| B. | 化学反应速率越大,说明单位时间内物质的量变化越大 | |
| C. | 对于可逆反应,达到平衡时正逆反应速率相等且等于零 | |
| D. | 改变适当的条件,可使化学平衡向需要的方向移动 |
13.钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源等领域.工业上利用冶炼铝生成的固体废料--赤泥(主要成份为Fe2O3、Al2O3、V2O5及少量稀土金属氧化物)提取金属钒,其工艺流程图如下:

已知:钒有多种价态,其中+5价最稳定.钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O?VO3-+2H+.下列说法正确的是( )

已知:钒有多种价态,其中+5价最稳定.钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O?VO3-+2H+.下列说法正确的是( )
| A. | 工业生产中,碱浸步骤可选用较为廉价的氨水 | |
| B. | 可以推测VO2Cl溶解度大于NH4VO3 | |
| C. | 焙烧非磁性产品所得的固体产物加酸溶解时,应加入过量盐酸以使其溶解完全 | |
| D. | 将磁性产品加入稀硝酸溶解,取上层清液再加入KSCN溶液后未见血红色,则磁性产品中一定不含铁元素 |
20.向盛有硫酸铜溶液的试管中加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色透明溶液.下列对此现象的相关说法不正确的是( )
| A. | 沉淀溶解后,生成深蓝色的配离子为[Cu(NH3)4]2+ | |
| B. | 向反应后的溶液中加入乙醇,有沉淀析出 | |
| C. | 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对 | |
| D. | 反应前后,Cu2+浓度不变 |
17.下列有关煤、石油、天然气等资源的说法正确的是( )
| A. | 石油裂解得到的汽油是纯净物 | B. | 煤就是碳,属于单质 | ||
| C. | 煤的气化是物理变化过程 | D. | 天然气是一种清洁的化石燃料 |
14.下列有关化学用语表示正确的是( )
| A. | CSO的电子式: | |
| B. | 甲烷分子的球棍模型: | |
| C. | 2-戊烯的结构简式CH3CH2CHCHCH3 | |
| D. | HCO3-的水解方程式为:HCO3-+H2O?CO32-+H3O+ |
 .完成下列问题:
.完成下列问题: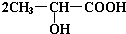 +Na2CO3→
+Na2CO3→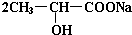 +H2O+CO2↑.
+H2O+CO2↑.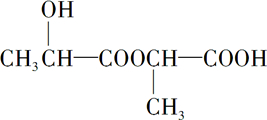 .
.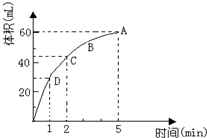 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示,5分钟时反应停止.请依图回答下列问题:
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示,5分钟时反应停止.请依图回答下列问题: