题目内容
现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命体不可缺少的重要元素,已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e,B、D、E都有多种同素异形体.B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但有一点是肯定的,那就是没有第三种元素的化合物种数会超出它们.根据以上信息回答下列有关问题:
(1)B的化合物种类繁多的原因是 .
(2)请判断B2A4、C2A4、E2A4三种化合物中沸点最高的是 .
(3)以题中给定的元素为选择对象组成物质,写出一个置换反应的化学方程式: .
(4)从题中给定的元素中选出若干种组成化合物,写出三种完全燃烧时生成CO2和H2O的物质的量之比为1:2的化合物的名称 .
(1)B的化合物种类繁多的原因是
(2)请判断B2A4、C2A4、E2A4三种化合物中沸点最高的是
(3)以题中给定的元素为选择对象组成物质,写出一个置换反应的化学方程式:
(4)从题中给定的元素中选出若干种组成化合物,写出三种完全燃烧时生成CO2和H2O的物质的量之比为1:2的化合物的名称
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但有一点是肯定的,那就是没有第三种元素的化合物种数会超出它们,则B、A为C或H,又B有多种同素异形体,则B为C,A为H;
a+b=c,即:C的原子序数为:c=1+6=7,则C为N元素;
a+c=d,D的原子序数为:d=1+7=8,则D为O元素;
c+d=e,E的原子序数为:e=7+8=15,则E为P元素,
依据分析可知:A为H、B为C元素、C为N元素、D为O元素、E为P元素,据此解答各小题即可.
a+b=c,即:C的原子序数为:c=1+6=7,则C为N元素;
a+c=d,D的原子序数为:d=1+7=8,则D为O元素;
c+d=e,E的原子序数为:e=7+8=15,则E为P元素,
依据分析可知:A为H、B为C元素、C为N元素、D为O元素、E为P元素,据此解答各小题即可.
解答:
解:B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但有一点是肯定的,那就是没有第三种元素的化合物种数会超出它们,则B、A为C或H,又B有多种同素异形体,则B为C,A为H;a+b=c,即:C的原子序数为:c=1+6=7,则C为N元素;a+c=d,D的原子序数为:d=1+7=8,则D为O元素;c+d=e,E的原子序数为:e=7+8=15,则E为P元素,
则:A为H、B为C元素、C为N元素、D为O元素、E为P元素,
(1)B为C元素,碳原子连接方式多样可以是链状、也可以是环状;同种分子也可以有不同的结构,所以有机物种类繁多,
故答案为:碳原子连接方式多样、同分异构现象;
(2)B2A4、C2A4、E2A4三种化合物分别为C2H4、N2H4、P2H4,都为分子晶体,相对分子质量越大,沸点越高,但由于氮元素电负性很强,所以N2H4中存在氢键,沸点相对更高,所以沸点由高到低的顺序为:N2H4>P2H4>C2H4,
故答案为:N2H4>P2H4>C2H4;
(3)碳与水在高温下反应生成CO和氢气,反应的化学方程式为:C+H2O
CO+H2,
故答案为:C+H2O
CO+H2;
(4)完全燃烧时生成CO2和H2O的物质的量之比为1:2,则分子中C、H原子数之比为1:4,如果为烃,则C、H数之比为1:4的为甲烷;
若为含氧衍生物,则可以为甲醇;还可能为醋酸铵:(NH4)2C2O4,
故答案为:甲烷、甲醇、醋酸铵.
则:A为H、B为C元素、C为N元素、D为O元素、E为P元素,
(1)B为C元素,碳原子连接方式多样可以是链状、也可以是环状;同种分子也可以有不同的结构,所以有机物种类繁多,
故答案为:碳原子连接方式多样、同分异构现象;
(2)B2A4、C2A4、E2A4三种化合物分别为C2H4、N2H4、P2H4,都为分子晶体,相对分子质量越大,沸点越高,但由于氮元素电负性很强,所以N2H4中存在氢键,沸点相对更高,所以沸点由高到低的顺序为:N2H4>P2H4>C2H4,
故答案为:N2H4>P2H4>C2H4;
(3)碳与水在高温下反应生成CO和氢气,反应的化学方程式为:C+H2O
| ||
故答案为:C+H2O
| ||
(4)完全燃烧时生成CO2和H2O的物质的量之比为1:2,则分子中C、H原子数之比为1:4,如果为烃,则C、H数之比为1:4的为甲烷;
若为含氧衍生物,则可以为甲醇;还可能为醋酸铵:(NH4)2C2O4,
故答案为:甲烷、甲醇、醋酸铵.
点评:本题考查了位置、结构与性质关系的综合应用,题目难度中等,正确推断各元素名称为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
相关题目
已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是( )
| A、该反应中还原剂为Fe2+,O2、Fe(OH)3均为氧化产物 |
| B、若有4molNa2O2参加反应,则反应中共得到8NA个电子 |
| C、标准状况下,每生成22.4LO2,则有4molNa2O2被还原 |
| D、反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀 |
下列物质分子的电子式正确的是( )
A、CH3Cl  |
B、羟基 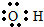 |
C、CO2  |
D、C2H4 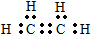 |
假设SiO2原子晶体中的Si原子被Al原子取代,不足的价数用K原子补充.当有25%的Si原子取代时,可形成正长石,则正长石的化学组成为( )
| A、KAlSiO4 |
| B、KAlSi2O4 |
| C、KAlSi3O8 |
| D、KAlSi4O10 |
下列单体能在一定条件下加聚反应生成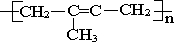 的是( )
的是( )
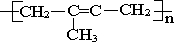 的是( )
的是( )| A、丙烯 |
| B、2-甲基-1,3-丁二烯 |
| C、乙烯和丙烯 |
| D、2-甲基-2-丁烯 |