题目内容
14.下列关于硫及含硫化合物的叙述不正确的是( )| A. | SO2能使品红溶液褪色 | |
| B. | 硫在空气中燃烧生成大量SO3 | |
| C. | 浓硫酸用作干燥剂 | |
| D. | 常温下铝遇浓硫酸钝化,因此可用铝槽车储运浓硫酸 |
分析 A、根据SO2漂白原理;
B、根据硫的可燃性;
C、根据浓硫酸的吸水性,可作干燥剂;
D、根据钝化在表面生成一层致密的氧化膜,阻止反应进行.
解答 解:A、SO2具有漂白性,能够和某些有色物质结合生成无色物质,但是不能漂白酸碱指示剂,能使品红溶液褪色,故A正确;
B、因硫在空气中燃烧生成SO2,不会生成SO3,故B错误;
C、根据浓硫酸的吸水性,可作干燥剂,故C正确;
D、铁和铝会与浓硫酸发生钝化,在表面生成一层致密的氧化膜,阻止反应进行,因此可以用铝槽车储运浓硫酸,故D正确;
故选B.
点评 本题主要考查了元素及其化合物的有关知识,试题有一定的难度.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
15.下列烷烃中,能由相应的炔烃与 H2加成制得的是( )
| A. |  | B. |  | C. | 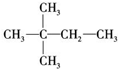 | D. | 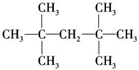 |
16.加热金属Cu与浓硫酸反应,得到SO2的体积为2.24L(标准状况).则( )
| A. | 被还原的H2SO4为0.2moL | |
| B. | 反应中共转移电子0.1moL | |
| C. | 反应消耗了金属Cu6.4g | |
| D. | 生成的CuSO4配成500mL溶液,浓度为1mol/L |
2.氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)BCl3的空间构型为;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A. CsICl2═CsCl+ICl
B. CsICl2═CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是I.
(4)下列分子既不存在s-pσ键,也不存在p-pπ键的是D.
A. HCl B.HF C.CO2 D. SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3杂化,写出CN-的等电子体的分子式(写出1个)N2或CO.
(6)由H、N、O三种元素组成的常用作化肥,且水溶液显酸性化合物固态时属于离子晶体,假设其晶体的空间结构与氯化钠相似,且晶胞的棱长为acm,则该晶胞的密度为$\frac{320}{{N}_{A}•{a}^{3}}$g/cm3.
(1)BCl3的空间构型为;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A. CsICl2═CsCl+ICl
B. CsICl2═CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是I.
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(KJ/mol) | 1681 | 1251 | 1140 | 1008 |
A. HCl B.HF C.CO2 D. SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3杂化,写出CN-的等电子体的分子式(写出1个)N2或CO.
(6)由H、N、O三种元素组成的常用作化肥,且水溶液显酸性化合物固态时属于离子晶体,假设其晶体的空间结构与氯化钠相似,且晶胞的棱长为acm,则该晶胞的密度为$\frac{320}{{N}_{A}•{a}^{3}}$g/cm3.
19.下列实验装置图正确的是( )
| A. | 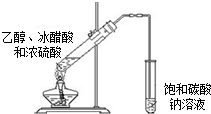 实验室制取乙酸乙酯 | B. | 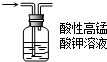 除去乙烷中的乙烯 | ||
| C. | 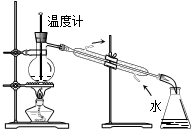 分离甲苯与乙醇 | D. | 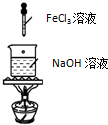 制备Fe(OH)3胶体 |
6.下列反应中,属于加成反应的是( )
| A. | CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl | |
| B. | CH2=CH2+HOCl$\stackrel{催化剂}{→}$HOCH2-CH2Cl | |
| C. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| D. | 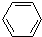 +Br2$\stackrel{催化剂}{→}$ +Br2$\stackrel{催化剂}{→}$ -Br+HBr -Br+HBr |
3.关于钠与水反应的现象,下列说法错误的是( )
| A. | 钠熔化成银白色小球 | B. | 钠沉在水底 | ||
| C. | 反应剧烈 |
4.关于如图所示的装置叙述正确的是( )
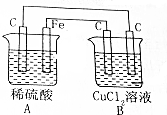

| A. | 装置A是电解池,装置B是原电池 | |
| B. | 装置A是原电池,装置B是电解池 | |
| C. | 电子由装置A中碳棒流向装置B中碳棒 | |
| D. | 工作一段时间后,A装置中稀H2SO4溶液质量减轻,B装置中CuCl2质量减轻 |