题目内容
 过碳酸钠是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,化学式可表示为aNa2CO3?bH2O2,具有Na2CO3和H2O2的性质.某化学兴趣小组进行如下实验:
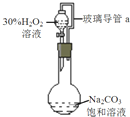
过碳酸钠是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,化学式可表示为aNa2CO3?bH2O2,具有Na2CO3和H2O2的性质.某化学兴趣小组进行如下实验:实验I 制备过碳酸钠用图装置和药品制备过碳酸钠,反应为:aNa2CO3+bH2O2=aNa2CO3?bH2O2,△H<0
(1)图中玻璃导管a的作用是
(2)该反应要控制在较低的温度下进行,其原因是
(3)用该装置制备过碳酸钠有不足之处,下列改进措施可行的是
①缓慢滴加H2O2溶液 ②添加冷却装置 ③用酒精灯加热
实验Ⅱ探究过碳酸钠的性质
(4)为探究Na2CO3对H2O2稳定性的影响设计实验,请完善如下实验方案:
①取等体积、等浓度的H2O2溶液于两支试管中;
②
③在两支试管中分别加人等量MnO2粉末;
④
实验Ⅲ测定过碳酸钠中H2O2的质量分数
KMnO4滴定过碳酸钠的原理:
6KMnO4+5(aNa2CO3?bH2O2)+19H2SO4═3K2SO4+6MnSO4+5aNa2SO4+5aCO2↑+15O2↑+34H2O
(5)分析上述反应可得a=
(6)准确称取实验制得的过碳酸钠0.2000g于250mL锥形瓶中,加50mL蒸馏水溶解,再加50mL2.0mol?L-1 H2SO4,用2.000x10-2 mol?L-1 KMnO4标准溶液滴定至终点时消耗30.00mL,则所制得的过碳酸钠中H2O2的质量分数为
考点:性质实验方案的设计,探究碳酸钠与碳酸氢钠的性质
专题:实验设计题
分析:(1)通过玻璃导管a可以使圆底烧瓶与分液漏斗中的压强相等;
(2)双氧水不稳定,温度稍高时水分解生成水和氧气;
(3)根据该反应需要在低温下进行判断反应条件;
(4)根据实验目的为“探究Na2CO3对H2O2稳定性的影响”,然后根据对照实验的设计方法进行设计该实验方案;
(5)先根据氢原子守恒计算出b,然后根据氧原子守恒计算出a;
(6)先写出反应的化学方程式,然后根据双氧水与高锰酸钾的物质的量关系计算出样品中双氧水的百分含量.
(2)双氧水不稳定,温度稍高时水分解生成水和氧气;
(3)根据该反应需要在低温下进行判断反应条件;
(4)根据实验目的为“探究Na2CO3对H2O2稳定性的影响”,然后根据对照实验的设计方法进行设计该实验方案;
(5)先根据氢原子守恒计算出b,然后根据氧原子守恒计算出a;
(6)先写出反应的化学方程式,然后根据双氧水与高锰酸钾的物质的量关系计算出样品中双氧水的百分含量.
解答:
解:(1)图中玻璃导管a的作用是使圆底烧瓶与分液漏斗相通,起到平衡压强的作用,
故答案为:平衡压强;
(2)双氧水容易分解,反应的化学方程式为:2H2O2
2H2O+O2↑,影响过碳酸钠的制备效率,所以该反应要控制在较低的温度下进行,
故答案为:2H2O2
2H2O+O2↑;
(3)制备过碳酸钠需要在低温下进行,由于反应aNa2CO3+bH2O2=aNa2CO3?bH2O2,△H<0为放热反应,则需要缓缓滴加双氧水,以便降低反应放出的热量对双氧水分解的影响;还需要添加冷却装置,但不能在加热条件下进行,所以①②正确,
故答案为:①②;
(4)为探究Na2CO3对H2O2稳定性的影响设计实验方案为:首先①取等体积、等浓度的H2O2溶液于两支试管中;
然后②往其中一只试管中加入少量碳酸钠;
再③在两支试管中分别加人等量MnO2粉末;
最后④观察两只试管中气泡产生的快慢,据此判断碳酸钠对双氧水稳定性的影响,
故答案为:故答案为:往其中一只试管中加入少量碳酸钠;观察两只试管中气泡产生的快慢;
(5)6KMnO4+5(aNa2CO3?bH2O2)+19H2SO4═3K2SO4+6MnSO4+5aNa2SO4+5aCO2↑+15O2↑+34H2O,根据H原子守恒可得:5b×2+19×2=34×2,解得b=3;再根据氧原子守恒可得:6×4+5a×3+5×3×2+19×4=3×4+6×4+5a×4+5a×2+15×2+34,解得:a=2、b=3,
故答案为:a=2,b=3;
(6)高锰酸钾溶液与过碳酸钠反应的化学方程式为:6KMnO4+5(2Na2CO3?3H2O2)+19H2SO4═3K2SO4+6MnSO4+10Na2SO4+10CO2↑+15O2↑+34H2O,滴定过程中消耗2.000x10-2 mol?L-1 KMnO4标准溶液的物质的量为:2.000x10-2 mol?L-1×0.03L=6.000x10-4mol,
则所制得的过碳酸钠中H2O2的质量分数为:
×100%=25.5%,
故答案为:25.5%.
故答案为:平衡压强;
(2)双氧水容易分解,反应的化学方程式为:2H2O2
| ||
故答案为:2H2O2
| ||
(3)制备过碳酸钠需要在低温下进行,由于反应aNa2CO3+bH2O2=aNa2CO3?bH2O2,△H<0为放热反应,则需要缓缓滴加双氧水,以便降低反应放出的热量对双氧水分解的影响;还需要添加冷却装置,但不能在加热条件下进行,所以①②正确,
故答案为:①②;
(4)为探究Na2CO3对H2O2稳定性的影响设计实验方案为:首先①取等体积、等浓度的H2O2溶液于两支试管中;
然后②往其中一只试管中加入少量碳酸钠;
再③在两支试管中分别加人等量MnO2粉末;
最后④观察两只试管中气泡产生的快慢,据此判断碳酸钠对双氧水稳定性的影响,
故答案为:故答案为:往其中一只试管中加入少量碳酸钠;观察两只试管中气泡产生的快慢;
(5)6KMnO4+5(aNa2CO3?bH2O2)+19H2SO4═3K2SO4+6MnSO4+5aNa2SO4+5aCO2↑+15O2↑+34H2O,根据H原子守恒可得:5b×2+19×2=34×2,解得b=3;再根据氧原子守恒可得:6×4+5a×3+5×3×2+19×4=3×4+6×4+5a×4+5a×2+15×2+34,解得:a=2、b=3,
故答案为:a=2,b=3;
(6)高锰酸钾溶液与过碳酸钠反应的化学方程式为:6KMnO4+5(2Na2CO3?3H2O2)+19H2SO4═3K2SO4+6MnSO4+10Na2SO4+10CO2↑+15O2↑+34H2O,滴定过程中消耗2.000x10-2 mol?L-1 KMnO4标准溶液的物质的量为:2.000x10-2 mol?L-1×0.03L=6.000x10-4mol,
则所制得的过碳酸钠中H2O2的质量分数为:
34g/mol×(6.000×10-4mol×
| ||
| 0.2000g |
故答案为:25.5%.
点评:本题考查了性质实验方案的设计、化学方程式书写、物质质量分数的计算等知识,题目难度较大,注意掌握设计化学实验方案的方法,能够根据反应方程式进行简单的化学计算,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
某温度下,将Cl2通入KOH溶液中得KCl、KClO3和KClO的混合溶液.经测定ClO3-和ClO-物质的量之比为2:1,则反应中被还原的Cl2与被氧化Cl2的物质的量之比为( )
| A、2:3 | B、3:4 |
| C、11:3 | D、10:3 |
下列有机实验操作或叙述正确的是( )
| A、将乙烯和乙炔气体分别通入溴的四氯化碳溶液中前者退色,后者不退色 |
| B、甲烷和氯气在室温下的黑暗环境中可以稳定存在 |
| C、苯能使溴水退色是因为二者反应生成了溴苯 |
| D、要除去乙烷中的乙烯制得纯净的乙烷,可将混合气通入酸性高锰酸钾溶液中 |
 如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,回答下问题:
如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,回答下问题: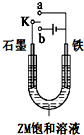 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答: