题目内容
10.Na2CO3和NaHCO3是两种常见的化工原料.(1)取少量碳酸钠固体溶于水,滴加酚酞试液后溶液呈红色,加热后溶液红色变深,请结合有关方程式用平衡移动原理进行解释CO32-+H2O?HCO3-+OH-,水解为吸热过程,加热促进水解平衡正向移动.若将CuSO4溶液投入到NaHCO3饱和溶液中,立即产生大量气体生成,同时得到蓝绿色的沉淀Cu2(OH)2CO3,反应的离子方程式为2Cu2++4HCO3-═Cu2(OH)2CO3↓+3CO2↑+H2O.
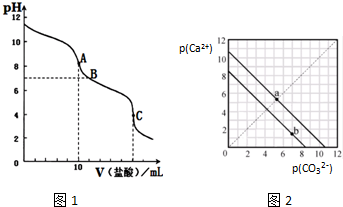
(2)用0.1000mol•L-1的盐酸滴定10.00mL 0.1000mol•L-1的碳酸钠溶液,溶液pH值与加入盐酸的体积的关系如图1所示.已知室温时饱和CO2溶液的pH约为3.9,0.05mol•L-1 NaHCO3的pH约为8.3.
①准确量取10.00mL0.1000mol•L-1的碳酸钠溶液所用的仪器为(碱式)滴定管或移液管,用甲基橙为指示剂滴定到C点时,滴定终点现象为最后一滴盐酸加入时,溶液由黄色变成橙色(半分钟不变色).
②当盐酸用量为5mL时,溶液中c(CO32-)<c(HCO3-);水的电离程度比较:A点>C点(填“>”、“<”或“=”).
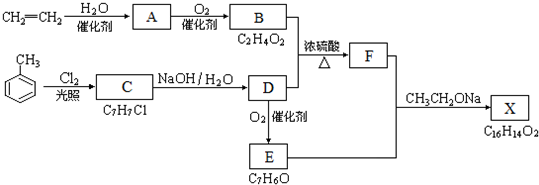
(3)已知25℃时CaCO3的Ksp=2.8×10-9.若将浓度为2×10-4 mol•L-1Na2CO3溶液与CaCl2溶液等体积混合生成CaCO3沉淀,则混合前CaCl2溶液的最小浓度为5.6×10-5mol•L-1.已知CaCO3溶解是吸热过程,p(Ca2+)=-lgc(Ca2+),p(CO32-)=-lgc(CO32-),若b点温度为25℃,则图2中a点温度<25℃(填“>”、“<”或“相等”).
分析 (1)加热后溶液红色变深,说明加热促进水解,水解平衡正向移动;CuSO4溶液投入到NaHCO3饱和溶液中,铜离子与碳酸氢根离子水解相互促进;
(2)①准确量取10.00mL0.1000mol•L-1的碳酸钠溶液,因碳酸钠溶液水解呈碱性,所用的仪器为 碱式滴定管或移液管,用甲基橙为指示剂滴定到C点时,因未滴定时溶液呈碱性,所以滴定终点现象为溶液由黄色变成橙色;
②当盐酸用量为5mL时,得到等物质量浓度的碳酸钠和碳酸氢钠溶液,碳酸根离子的水解程度大于碳酸氢根离子,溶液中c(CO32-)<c(HCO3-);水的电离程度比较:A点是恰好完全反应生成碳酸氢钠,而C点是酸过量;
(3)CaCl2溶液的最小浓度时即钙离子与碳酸根离子达溶解平衡状态,设CaCl2溶液的最小浓度为x,则2×10-4×$\frac{1}{2}$×x×$\frac{1}{2}$=2.8×10-9,解之得x=5.6×10-5mol•L-1,由p(Ca2+)=-lgc(Ca2+),p(CO32-)=-lgc(CO32-)可知,p越大对就离子浓度越小,而a的p值大于b所以a点的Ksp较小,电离平衡逆向移动,温度降低.
解答 解:(1)碳酸钠是强碱弱酸盐,碳酸根离子水解CO32-+H2O?HCO3-+OH-:加热后溶液红色变深,说明加热促进水解,水解平衡正向移动;CuSO4溶液投入到NaHCO3饱和溶液中,铜离子与碳酸氢根离子水解相互促进,反应的化学方程式为:2Cu2++4HCO3-═Cu2(OH)2CO3↓+3CO2↑+H2O;故答案为:CO32-+H2O?HCO3-+OH-,水解为吸热过程,加热促进水解平衡正向移动;2Cu2++4HCO3-═Cu2(OH)2CO3↓+3CO2↑+H2O;
(2))①准确量取10.00mL0.1000mol•L-1的碳酸钠溶液,因碳酸钠溶液水解呈碱性,所用的仪器为 碱式滴定管或移液管,用甲基橙为指示剂滴定到C点时,因未滴定时溶液呈碱性,所以滴定终点现象为溶液由黄色变成橙色;,故答案为:(碱式)滴定管或移液管;最后一滴盐酸加入时,溶液由黄色变成橙色(半分钟不变色);
②当盐酸用量为5mL时,得到等物质量浓度的碳酸钠和碳酸氢钠溶液,碳酸根离子的水解程度大于碳酸氢根离子,溶液中c(CO32-)<c(HCO3-);水的电离程度比较:A点是恰好完全反应生成碳酸氢钠,碳酸氢钠的水解对水的电离起促进作用,而C点是酸过量,酸对水的电离起抑制作用,所以水的电离程度比较:A点>C点;故答案为:<;>;
(3)CaCl2溶液的最小浓度时即钙离子与碳酸根离子达溶解平衡状态,设CaCl2溶液的最小浓度为x,则2×10-4×$\frac{1}{2}$×x×$\frac{1}{2}$=2.8×10-9,解之得x=5.6×10-5mol•L-1,由p(Ca2+)=-lgc(Ca2+),p(CO32-)=-lgc(CO32-)可知,p越大对就离子浓度越小,而a的p值大于b所以a点的Ksp较小,电离平衡逆向移动,温度降低,故答案为:5.6×10-5;<.
点评 本题主要考查了沉淀溶解平衡曲线,掌握图线中pc(CO32-)、pM数值越大,实际浓度越小是解题的关键,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 一定条件下,2mol SO2与足量O2反应可得到2mol SO3 | |
| B. | 含4mol HCl 的浓盐酸与足量的MnO2加热反应可制备1mol Cl2 | |
| C. | 10ml 18.0 mol/L H2SO4与足量铜加热反应可制备0.09 mol SO2 | |
| D. | 一定条件下,1mol N2与3 mol H2反应可制备1.0 mol NH3 |
| A. | 生石灰-Ca(OH)2 | B. | 小苏打-KHCO3 | C. | 重晶石-CaSO4 | D. | 醋酸-C2H4O2 |
| A. | 原子半径:W<Y<Z | |
| B. | 简单气态氢化物的热稳定性:Z>Y>W | |
| C. | W、X能形成两种化合物,其中一种与水反应生成气体 | |
| D. | 四种元素中,Z的最高价氧化物对应的水化物酸性最强 |
| A. | CuS | B. | FeCl2 | C. | Cu2S | D. | Fe2S3 |
 ;
; ;
; B、
B、
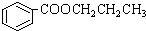
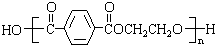 ,其合成单体为
,其合成单体为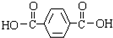 和HOCH2CH2OH;
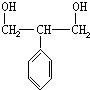
和HOCH2CH2OH;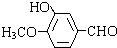 )的重要原料,写出同时满足下列条件的M的同分异构体的结构简式:
)的重要原料,写出同时满足下列条件的M的同分异构体的结构简式: .
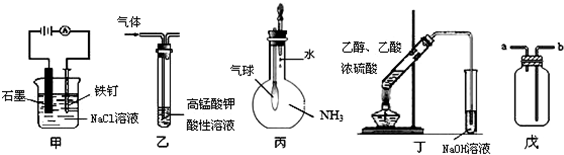
.
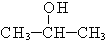 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O,产物不发生银镜反应;
+2H2O,产物不发生银镜反应; +H2$→_{△}^{催化剂}$
+H2$→_{△}^{催化剂}$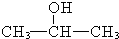 .
.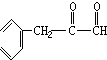 ,G与M是由不同方式形成的高分子化合物.
,G与M是由不同方式形成的高分子化合物.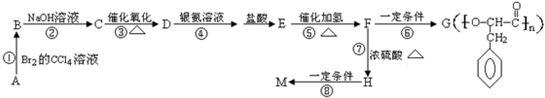
 .
.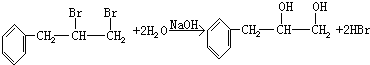 ,取代反应;
,取代反应; ,加聚反应.
,加聚反应.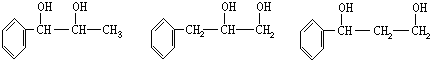
 ,
,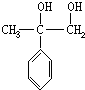 .
.