题目内容
某同学为了探究氯气的有关性质,设计了如图所示装置进行实验: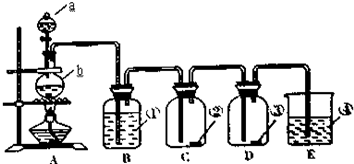
其中①为饱和食盐水;②为干燥的红纸条;③为干燥KI淀粉试纸;④为氢氧化钠溶液.
请回答:(1)写出a仪器的名称 ;
(2)描述该装置气密性的检查方法 ;
(3)写出E中发生反应的化学方程式 ;
(4)该同学按他设计的装置进行实验,发现干燥的红色纸条的颜色也很快褪去.请分析出现此现象的原因: ;
(5)D中可能观察到的现象 ;
(6)实验结束时,为了防止倒吸,该同学先将导管从NaOH溶液中移出液面,然后再移去酒精灯,会造成的影响是 .

其中①为饱和食盐水;②为干燥的红纸条;③为干燥KI淀粉试纸;④为氢氧化钠溶液.
请回答:(1)写出a仪器的名称
(2)描述该装置气密性的检查方法
(3)写出E中发生反应的化学方程式
(4)该同学按他设计的装置进行实验,发现干燥的红色纸条的颜色也很快褪去.请分析出现此现象的原因:
(5)D中可能观察到的现象
(6)实验结束时,为了防止倒吸,该同学先将导管从NaOH溶液中移出液面,然后再移去酒精灯,会造成的影响是
考点:氯气的实验室制法,氯、溴、碘的性质实验
专题:实验题
分析:(1)依据装置图中仪器和用途分析,a为分液漏斗;
(2)装置气密性的检查方法,保持装置密闭,微热烧瓶,观察E烧杯中导气管中汽包冒出,停止加热,一段水柱上升;
(3)E中发生反应是利用氢氧化钠溶液吸收氯气反应生成氯化钠、次氯酸钠和水;
(4)发现干燥的红色纸条的颜色也很快褪去,说明进入的氯气含有水蒸气,生成次氯酸具有漂白性;
(5)D装置中是碘化钾淀粉试纸,通入湿润的氯气,氯气氧化碘离子为碘单质,遇到淀粉变蓝;
(6)氯气有毒排放到空气中会污染空气;
(2)装置气密性的检查方法,保持装置密闭,微热烧瓶,观察E烧杯中导气管中汽包冒出,停止加热,一段水柱上升;
(3)E中发生反应是利用氢氧化钠溶液吸收氯气反应生成氯化钠、次氯酸钠和水;
(4)发现干燥的红色纸条的颜色也很快褪去,说明进入的氯气含有水蒸气,生成次氯酸具有漂白性;
(5)D装置中是碘化钾淀粉试纸,通入湿润的氯气,氯气氧化碘离子为碘单质,遇到淀粉变蓝;
(6)氯气有毒排放到空气中会污染空气;
解答:
解:(1)依据装置图中仪器和用途分析,a为分液漏斗;
故答案为:分液漏斗;
(2)装置气密性的检查方法,保持装置密闭,微热烧瓶,观察E烧杯中导气管中汽包冒出,停止加热,一段水柱上升;
故答案为:关闭分液漏斗活塞,安图连接装置,最后的烧杯中加入水,微热烧瓶,观察E烧杯中导气管中汽包冒出,停止加热,一段水柱上升,气密性完好;
(3)E中发生反应是利用氢氧化钠溶液吸收氯气反应生成氯化钠、次氯酸钠和水,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(4)发现干燥的红色纸条的颜色也很快褪去,说明进入的氯气含有水蒸气,生成次氯酸具有漂白性;
故答案为:氯气含有水蒸气,氯气和水反应生成次氯酸;
(5)D装置中是碘化钾淀粉试纸,通入湿润的氯气,氯气氧化碘离子为碘单质,遇到淀粉变蓝;
故答案为:试纸变蓝色;
(6)实验结束时,为了防止倒吸,该同学先将导管从NaOH溶液中移出液面,然后再移去酒精灯,会造成的影响是,氯气有毒排放到空气中会污染空气;
故答案为:氯气有毒,会污染空气;
故答案为:分液漏斗;
(2)装置气密性的检查方法,保持装置密闭,微热烧瓶,观察E烧杯中导气管中汽包冒出,停止加热,一段水柱上升;
故答案为:关闭分液漏斗活塞,安图连接装置,最后的烧杯中加入水,微热烧瓶,观察E烧杯中导气管中汽包冒出,停止加热,一段水柱上升,气密性完好;
(3)E中发生反应是利用氢氧化钠溶液吸收氯气反应生成氯化钠、次氯酸钠和水,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(4)发现干燥的红色纸条的颜色也很快褪去,说明进入的氯气含有水蒸气,生成次氯酸具有漂白性;
故答案为:氯气含有水蒸气,氯气和水反应生成次氯酸;
(5)D装置中是碘化钾淀粉试纸,通入湿润的氯气,氯气氧化碘离子为碘单质,遇到淀粉变蓝;
故答案为:试纸变蓝色;
(6)实验结束时,为了防止倒吸,该同学先将导管从NaOH溶液中移出液面,然后再移去酒精灯,会造成的影响是,氯气有毒排放到空气中会污染空气;
故答案为:氯气有毒,会污染空气;
点评:本题考查了实验室制备氯气的方法分析,装置图中试剂作用,主要是氯气性质的分析判断,注意干燥氯气无漂白性,题目难度中等.

练习册系列答案
相关题目
NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、1.0L 1.0mol?L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| B、1mol醋酸的质量与NA个醋酸分子的质量一定相等 |
| C、2.24L CO2中含有的原子数为0.3NA |
| D、0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA |
下列不属于取代反应的是( )
A、CH4+Cl2
| |||
B、CH3Cl+Cl2
| |||
C、CH4+2O2
| |||
D、CH2=CH2+H2
|
下列条件的变化,是因为降低反应所需的能量而增加单位体积内的反应物活化分子百分数致使反应速率加快的是( )
| A、增大浓度 | B、增大压强 |
| C、升高温度 | D、使用催化剂 |
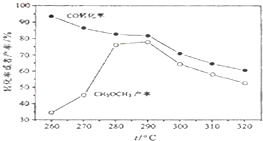 (除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图:
(除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图: