题目内容
25℃和101kPa时,甲烷、乙炔和乙烯组成的混合烃10mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小17.5mL,原混合烃中乙炔的体积分数为( )
| A、12.5% | B、25% |
| C、50% | D、75% |
考点:化学方程式的有关计算
专题:烃及其衍生物的燃烧规律
分析:发生反应分别为:CH4+2O2=CO2+2H2O?,C2H4+3O2=2CO2+2H2O,C2H2+
O2=2CO2+H2O,除去水蒸气,恢复到原来的温度和压强,根据反应方程式可知,CH4和C2H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,设CH4和C2H4一共为xmL,C2H2为ymL,利用气体体积缩小了17.5mL及混合气体的体积来列等式计算出乙炔的体积,进而计算乙炔的体积分数.
| 5 |
| 2 |
解答:
解:除去水蒸气,恢复到原来的温度和压强,则:
CH4+2O2=CO2+2H2O?△V
1 2 1 2
C2H4+3O2=2CO2+2H2O?△V
1 3 2 2
C2H2+
O2=2CO2+H2O△V
1 2.5 2 1.5
CH4和C2H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,
设CH4和C2H4一共为xmL,C2H2为ymL,则:
解之得x=5,y=5,
则原混合烃中乙炔的体积分数为
×100%=50%,
故选C.
CH4+2O2=CO2+2H2O?△V
1 2 1 2
C2H4+3O2=2CO2+2H2O?△V
1 3 2 2
C2H2+
| 5 |
| 2 |
1 2.5 2 1.5
CH4和C2H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,
设CH4和C2H4一共为xmL,C2H2为ymL,则:
|
解之得x=5,y=5,
则原混合烃中乙炔的体积分数为
| 5mL |
| 10mL |
故选C.
点评:本题考查混合物计算、化学方程式有关计算,关键是根据方程式判断体积变化,把甲烷与乙烯看作一个组分,从而转化为两组分混合,注意差量法的应用,难度中等.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
若NA为阿伏加德罗常数,已知某元素的阴离子Rn-的原子核中,中子数为A-x+n,其中A为原子的质量数,则m g Rn-中电子总数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列反应体系中,不属于可逆反应的是( )
| A、Cl2溶解于水 |
| B、氨气溶解于水 |
| C、工业合成氨 |
| D、水电解生成H2和O2与H2在O2中燃烧生成H2O |
在密闭容器中进行的可逆反应:N2+3H2?2NH3(正反应为放热反应)中,要使反应速率增大,可采取的措施是( )
| A、减小NH3的浓度 |
| B、增大N2的浓度 |
| C、减小压强 |
| D、降低温度 |
某铁的氧化物,用7.0mol/L的盐酸100mL在一定条件下恰好完全溶解,所得溶液中再通入0.56L标况下的Cl2时,刚好使溶液中的Fe2+全部转化为Fe3+,则该氧化物中Fe(+2价)与Fe(+3价)的物质的量之比为( )
| A、1:4 | B、2:1 |
| C、4:1 | D、3:4 |
某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A、能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
| B、与足量氢气反应生成苯乙烷 |
C、能发生加聚反应,生成物可用表示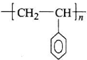 |
| D、易溶于水,也易溶于有机溶剂 |
下列化学用语使用正确的组合是( )
A、Mg2+结构示意图: | ||
B、含18个中子的氯原子的核素符号:
| ||
C、NH4Cl的电子式: | ||
D、四氯化碳分子球棍模型: |
 2SO2(g)+O2(g)═2SO3(g),反应过程的能量变化如图所示.已知:1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)═2SO3(g),反应过程的能量变化如图所示.已知:1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.