题目内容
9.关于如图所示各装置的叙述中,正确的是( )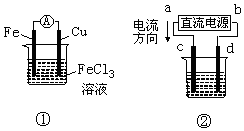
| A. | 装置①是原电池,总反应是:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 装置①中,铁做负极,该电极反应式为:Fe3++e-═Fe2+ | |
| C. | 装置②为铁上镀铜装置c为纯铜电极 | |
| D. | 若用装置②精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
分析 A.Fe比Cu的还原性强,Fe为负极;
B.Fe失去电子生成亚铁离子;
C.由电流从正极到负极可知,a为正极,c为阳极,铁上镀铜时Cu为阳极;
D.用装置②精炼铜,a为正极,粗铜作阳极.
解答 解:A.Fe比Cu的还原性强,Fe为负极,则装置①是原电池,总反应是Fe+2Fe3+═3Fe2+,故A错误;
B.Fe失去电子生成亚铁离子,则装置①中,铁做负极,该电极反应式为:Fe-2e-═Fe2+,故B错误;
C.由电流从正极到负极可知,a为正极,c为阳极,铁上镀铜时Cu为阳极,则c为纯铜电极,故C正确;
D.用装置②精炼铜,a为正极,粗铜作阳极,则c极为粗铜,d极为纯铜,电解质溶液为CuSO4溶液,故D错误;
故选C.
点评 本题考查原电池及电解池,为高频考点,把握装置、电极反应为解答的关键,侧重分析与应用能力的考查,注意电化学原理的应用,题目难度不大.

练习册系列答案
相关题目
19.下列物品所使用的主要材料,不属于有机合成材料的是( )
| A. |  塑料直尺 | B. |  尼龙提包 | C. |  纯羊毛手套 | D. |  塑胶地垫 |
17.某 KCl、MgCl2、Mg(NO3)2形成的混合溶液中,c(K+)=0.1mol•L-1,c( Mg2+)=0.25mol•L-1,c(Cl-)=0.2mol•L-1,则c(NO3-)为( )
| A. | 0.15 mol•L-1 | B. | 0.10 mol•L-1 | C. | 0.25 mol•L-1 | D. | 0.40 mol•L-1 |
4.当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
| A. | 当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 | |
| B. | 电池的正极反应式为:O2+2H2O+4e-═4OH- | |
| C. | 电解后电池中c(KOH)不变;c(Na2CO3)不变 | |
| D. | 电解后电解池中溶液pH变大,且溶液中有晶体析出 |
14.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 0.5 mol O3与11.2 L O2所含的分子数一定相等 | |
| C. | 物质的量浓度为0.5 mol/L MgCl2溶液,含有Cl-数为NA | |
| D. | 标况下,22.4 L四氯化碳的质量为154 g |
1.下列叙述涉及的化学相关知识,其中不正确的是( )
| A. | 打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释 | |
| B. | 用铁质自来水管与铜质水龙头连接使用时,连接处的铁水管锈蚀更快 | |
| C. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | |
| D. | 海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 |
18.在mA+nB=pC的反应中,(m、n、p为各物质的化学计量数)现测得C每分钟增加 2mol•L-1,B每分钟减少1.5mol•L-1,A每分钟减少0.5mol•L-1,则m:n:p为( )
| A. | 4:3:1 | B. | 2:2:3 | C. | 1:3:4 | D. | 3:1:2 |
19.下列有关非金属及其化合物的说法不正确的是( )
| A. | 二氧化硅是酸性氧化物,不与任何酸反应 | |
| B. | 将氯气通入紫色石蕊试液,先变红,后褪色 | |
| C. | 次氯酸不稳定,见光易分解 | |
| D. | SO2使紫色酸性高锰酸钾溶液褪色,体现了SO2强还原性 |