题目内容
下列说法正确的是( )
| A、酸性氧化物都是非金属氧化物 |
| B、碱性氧化物都是金属氧化物 |
| C、由同种元素构成的物质一定属于纯净物 |
| D、难溶于水的电解质一定是弱电解质 |
考点:混合物和纯净物,酸、碱、盐、氧化物的概念及其相互联系,电解质与非电解质
专题:
分析:A、酸性氧化物不一定是非金属氧化物;
B、碱性氧化物都是金属氧化物;
C、同种元素组成的单质可以是同素异形体;
D、不完全电离的属于弱电解质,与溶解度无关.
B、碱性氧化物都是金属氧化物;
C、同种元素组成的单质可以是同素异形体;
D、不完全电离的属于弱电解质,与溶解度无关.
解答:
解:A、酸性氧化物不一定是非金属氧化物,如Mn2O7,是酸性氧化物但却不是非金属氧化物,故A错误;
B、碱性氧化物都是金属氧化物,B正确;
C、同种元素组成的单质可以是同素异形体,如氧气和臭氧,故C错误;
D、不完全电离的属于弱电解质,与溶解度无关,故D错误,故选B.
B、碱性氧化物都是金属氧化物,B正确;
C、同种元素组成的单质可以是同素异形体,如氧气和臭氧,故C错误;
D、不完全电离的属于弱电解质,与溶解度无关,故D错误,故选B.
点评:本题考查了酸性氧化物与非金属氧化物、碱性氧化物与金属氧化物之间的辩证关系,难度不大.

练习册系列答案
相关题目
化学式与俗名相符的是( )
| A、烧碱Na2CO3 |
| B、胆矾CuSO4?5H2O |
| C、苏打NaHCO3 |
| D、纯碱NaOH |
下列有关说法正确的是( )
| A、金属氧化物都是碱性氧化物 |
| B、阴离子都只有还原性,金属阳离子都只有氧化性 |
| C、元素从化合态变为游离态时,一定失去电子,发生氧化反应 |
| D、人工固氮和漂白粉使石蕊溶液褪色都发生了氧化还原反应 |
下列物质的分类合理的是( )
| A、碱性氧化物:Na2O、CaO、MgO、Na2O2 |
| B、碱:NaOH、KOH、Ba(OH)2、Na2CO3 |
| C、铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3?H2O |
| D、非金属氧化物:CO2、NO、SO2、H2O |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、Na+结构示意图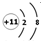 | ||||
B、质量数为16的氧原子:
| ||||
| C、纯碱的化学式:NaHCO3 | ||||
D、铁丝在氯气中燃烧的化学方程式:Fe+Cl2
|
科学家发现了如下反应:O2+PtF6═O2(PtF6),已知O2(PtF6)为离子化合物,Pt为+5价,下列说法正确的是( )
| A、O和F无正化合价 |
| B、1mol O2参加反应,转移1mol e- |
| C、上述反应中O2作氧化剂 |
| D、上述反应属于加成反应 |
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围: