题目内容
 罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图,已知断裂1molN-N吸收167kJ热量,生成1mol N≡N放出942kJ热量.根据以上信息和数据,估算由N2气体生成1mol气态N4的△H为( )
罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图,已知断裂1molN-N吸收167kJ热量,生成1mol N≡N放出942kJ热量.根据以上信息和数据,估算由N2气体生成1mol气态N4的△H为( )| A、+441kJ?mol-1 |
| B、+882kJ?mol-1 |
| C、-441kJ?mol-1 |
| D、-882kJ?mol-1 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:由N4分子结构可知,1molN4分子中含有6molN-N键,反应热等于反应物的总键能减去生成物的总键能,据此计算解答.
解答:
解:由题意知,N≡N的键能为942kJ/mol,N-N键的键能为167kJ/mol,
生成1molN4的反应为:2N2(g)=N4(g),反应热等于反应物的总键能减去生成物的总键能,
故反应热△H=2×942kJ/mol-6×167kJ/mol=+882kJ/mol,
故选B.
生成1molN4的反应为:2N2(g)=N4(g),反应热等于反应物的总键能减去生成物的总键能,
故反应热△H=2×942kJ/mol-6×167kJ/mol=+882kJ/mol,
故选B.
点评:本题考查根据键能进行反应热的有关计算,难度不大,注意掌握键能与反应热的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某反应:A?B+C 在低温下不能自发进行,在高温下能自发进行,对该反应过程△H、△S的判断正确的是( )
| A、△H<0、△S<0 |
| B、△H>0、△S<0 |
| C、△H<0、△S>0 |
| D、△H>0、△S>0 |
室温时,M(OH)2(s)?M2+(aq)+2OH-(aq).Ksp[M(OH)2]=a,c(M2+)=bmol?L-1时,溶液的pH等于( )
A、
| ||||
B、
| ||||
C、14+
| ||||
D、14+
|
对于下列反应类型的判断,不正确的是( )
| A、2FeCl2+Cl2═2FeCl3(化合反应) | ||||
B、3CO+Fe2O3
| ||||
C、2KClO3
| ||||
D、H2CO3
|
下列说法中正确的是( )
| A、放热反应在常温下都能自发进行 |
| B、Fe3++3H2O?Fe(OH)3+3H+是吸热反应 |
| C、熵值大小关系为:S(冰)>S(水)>S(水蒸气) |
| D、对C(s)+H2O(g)?CO(g)+H2(g),多加些炭可以提高化学反应速率 |
下列说法中错误的是( )
| A、根据对角线规则,铍和铝的性质具有相似性 |
| B、[Cu(H2O)4]2+中Cu提供空轨道,H2O中O提供孤对电子形成配位键 |
| C、元素电负性越大的原子,吸引电子的能力越强 |
| D、手性分子互为镜像,它们的性质没有区别 |
下列有关化学用语使用正确的是( )
A、氯原子的结构示意图: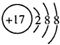 | ||
B、CO2分子的比例模型: | ||
C、具有10个中子的氧原子:
| ||
| D、乙烯的结构简式:C2H4 |
四种短周期元素在周期表中的位置如图,其中只有M为金属元素,下列说法不正确的是( )

| A、原子半径Z<M |
| B、Z位于元素周期表中第2周期、第ⅥA族 |
| C、X的最简单气态氢化物的热稳定性比Z的强 |
| D、Y的最高价氧化物对应水化物的酸性比X的强 |