题目内容
相同温度下,物质的量浓度均为1mol?L-1盐酸、硫酸、醋酸三种溶液,导电能力大小关系( )
| A、盐酸=硫酸=醋酸 |
| B、硫酸>盐酸>醋酸 |
| C、盐酸>硫酸>醋酸 |
| D、醋酸>盐酸>硫酸 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:溶液的导电性强弱主要取决于溶液中离子浓度的大小,离子浓度越大,导电性越强,还与离子所带电荷多少有关,相同浓度时,离子所带电荷越多,导电能能力越强.
解答:
解:相同物质的量浓度的盐酸、硫酸、醋酸三种溶液,醋酸是一元弱酸,是弱电解质,不能完全电离,盐酸是一元强酸,硫酸是二元强酸,能够完全电离,硫酸溶液中氢离子浓度是盐酸溶液中氢离子浓度的二倍,硫酸根离子和氯离子浓度虽然相同,但硫酸根带两个单位的电荷,而氯离子带一个单位的电荷,所以硫酸导电能力比盐酸强,盐酸比醋酸强,
故选B.
故选B.
点评:本题考查了溶液导电能力的强弱判断,注意导电性与离子浓度、离子电荷的关系即可解答,较简单.

练习册系列答案
相关题目
已知;HCN的K=4.9×10-10,H2CO3的K1=4.3×10-7,K2=5.6×10-11.判断等浓度的NaCN、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A、c(CN-)>c(HCO3-)>c(OH-)>c(H+) |
| B、c (CO32-)>c(CN-)>c(OH-)>c(H+) |
| C、c(CN-)+c(HCN)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D、c(Na+)+c(H+)=c(CN-)+c(HCO3-)+c(OH-)+c(CO32-) |
分子中具有手性碳原子的是 ( )
| A、甘油 |
| B、3-甲基己烷 |
| C、2-甲基-1-丁烯 |
| D、2,2-二甲基丙烷 |
等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)=2Z(g)+W(s)△H<0,下列叙述正确的是( )
| A、达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数 |
| B、达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动 |
| C、达到平衡时,反应速率v正(X)=2v逆(Z) |
| D、平衡常数K值越大,X的转化率越大 |
下列燃料中,不属于化石燃料的是( )
| A、煤 | B、石油 | C、天然气 | D、水煤气 |
下列说法错误的是( )
| A、用双氧水清洗伤口,可以杀菌消毒. |
| B、Na2O、Na2O2组成元素相同,但两者类别不同,与盐酸反应,产物也不同 |
| C、SO2是大气污染气体,直接排放会造成酸雨,向燃料煤中加入生石灰,可以减少对大气的污染 |
| D、往氯化铁饱和溶液中逐滴加入氨水,加热煮沸,可以制得氢氧化铁胶体 |
下列物质中有4种化学环境不同的氢的是( )
A、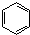 |
B、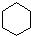 |
C、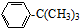 |
| D、CH3CH2CH(CH2CH3)2 |