题目内容
下列各组气体充分混合后,其平均相对分子质量可能为40的是( )
| A、NO和O2 |
| B、N2和O2 |
| C、SO2和CO2 |
| D、N2和NH3 |
考点:有关混合物反应的计算,物质的量的相关计算
专题:计算题
分析:题中只有NO和O2反应,气体混合后平均相对分子质量可能为40,则两种气体的相对分子质量分别小于40、大于40,以此解答该题.
解答:
解:A.NO和O2反应可生成NO2,其中NO和O2的相对分子质量都小于40,NO2的相对分子质量大于40,则气体充分混合后,其平均相对分子质量可能为40,故A正确;
B.N2和O2不反应,相对分子质量分别为28、32,都小于40,平均相对分子质量不可能为40,故B错误;
C.SO2和CO2不反应,相对分子质量分别为64、44,都大于40,平均相对分子质量不可能为40,故C错误;
D.N2和NH3不反应,相对分子质量分别为28、17,都小于40,平均相对分子质量不可能为40,故D错误.
故选A.
B.N2和O2不反应,相对分子质量分别为28、32,都小于40,平均相对分子质量不可能为40,故B错误;
C.SO2和CO2不反应,相对分子质量分别为64、44,都大于40,平均相对分子质量不可能为40,故C错误;
D.N2和NH3不反应,相对分子质量分别为28、17,都小于40,平均相对分子质量不可能为40,故D错误.
故选A.
点评:本题考查混合物的平均相对分子质量的考查,为高频考点,侧重于学生的分析、计算能力的考查,注意题目的答题角度,难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
下列化合物的沸点比较,前者低于后者的是( )
| A、乙醇与氯乙烷 |
B、 邻羟基苯甲酸与 邻羟基苯甲酸与 对羟基苯甲酸 对羟基苯甲酸 |
C、 对羟基苯甲醛与 对羟基苯甲醛与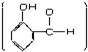 邻羟基苯甲醛 邻羟基苯甲醛 |
| D、H2O与H2Te |
设NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下,22.4LSO3含有NA个分子 |
| B、标准状况下,22.4LCO2与CO的混合气体含NA个分子 |
| C、lmolNa2O2与足量CO2反应转移的电子数为NA |
| D、常温下NA个H2分子的质量约为2g,它所占的体积约为22.4L |
向100mL 0.25mol?L-1的AlCl3溶液中,加入金属钠,恰好完全反应,形成只含有NaCl和NaAlO2的澄清溶液,则加入钠的物质的量应是( )
| A、0.025mol |
| B、0.05mol |
| C、0.1mol |
| D、0.25mol |
将0.56g铁粉加入到25mL 2mol?L-1的氯化铁溶液中,充分反应后其结果是( )
| A、铁有剩余,溶液呈浅绿色,Cl-浓度保持不变 |
| B、往溶液中滴无色KSCN溶液,溶液呈浅绿色 |
| C、Fe2+和Fe3+的物质的量之比为6:1 |
| D、氧化产物与还原产物的物质的量之比为1:2 |
为鉴别K2CO3和NaHCO3两种白色固体,下列4种方法中不可行的是( )
| A、分别取样配成溶液,滴加CaCl2溶液,观察有无白色沉淀 |
| B、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
| C、分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀 |
| D、分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
为除去FeSO4溶液中的Fe2(SO4)3和CuSO4,最好选用( )
| A、烧碱溶液 | B、浓氨水 |
| C、镁粉 | D、铁粉 |
