题目内容
6.以下性质的比较中,不正确的是( )| A. | 晶格能 NaCl<MgO | B. | 热稳定性:HF>H2O>NH3 | ||
| C. | 离子半径:Na+<O2- | D. | 第一电离能:P>Cl>S |
分析 A、离子所带电荷越多、离子半径越小,晶格能越大;
B、非金属性越强,对应氢化物越稳定;
C、相同电子层结构的不同微粒,原子序数越小半径越大;
D、同一周期中,元素的第一电离能随着原子序数的增大而增大.
解答 解:A、晶电荷越大,离子半径越小,则晶格能越大,则晶格能为NaCl<MgO,故A正确;
B、非金属性越强,对应氢化物越稳定,非金属性F>O>N,故热稳定性:HF>H2O>NH3,故B正确;
C、相同电子层结构的不同微粒,原子序数越小半径越大,故离子半径:Na+<O2-,故C正确;
D、同一周期中,元素的第一电离能随着原子序数的增大而增大,第一电离能:Cl>S>P,故D错误.
故选D.
点评 本题考查熔热稳定性、晶格能、离子半径、第一电离能,关键是理解掌握判断方法,理解概念,难度不大.

练习册系列答案
相关题目
16.有aX n+、b Ym-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
| A. | b-a=n+m | B. | a-b=n+m | C. | 核电荷数:Y>X | D. | 质子数:Y>X |
14.可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列表示放电时的负极反应的是( )
| A. | Zn-2e-=Zn2+ | B. | Br2+2e-=2Br- | C. | 2Br--2e-=Br2 | D. | Zn2++2e-=Zn |
1.下列各项所述的数字不是6的是( )
| A. | 在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数 | |
| B. | 在金刚石晶体中,围成最小环的原子数 | |
| C. | 在二氧化硅晶体中,围成最小环的硅原子数 | |
| D. | 在CsCl晶体中,与一个Cs+最近的且距离相等的Cl-的个数 |
11.下列各元素的氧化物中,既能与盐酸反应,又能与NaOH溶液反应的是( )
| A. | 元素X:它的原子中第三电子层比第二电子层少2个电子 | |
| B. | 元素Y:它的二价阳离子核外电子总数与氩原子相同 | |
| C. | 元素Z:位于元素周期表中的第3周期,ⅢA族 | |
| D. | 元素W:它的单质硬度最大 |
18.14C可用于考古,“14”是指( )
| A. | 质量数 | B. | 核外电子数 | C. | 中子数 | D. | 质子数 |
15.下列叙述中,错误的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持55℃-60℃反应生成硝基苯 | |
| B. | 苯在合适条件下催化加氢可生成环己烷 | |
| C. | 丙烯与溴的四氯化碳溶液反应生成1,2-二溴丙烷 | |
| D. | 甲苯与溴蒸气在光照条件下反应主要生成邻溴甲苯和对溴甲苯 |
16.下列关于苯的叙述中正确的是( )
| A. | 苯分子中碳碳键为单双键交替结构 | |
| B. | 苯中含有碳碳双键,所以苯属于烯烃 | |
| C. | 苯与氢气在一定条件下反应生成环己烷 | |
| D. | 苯可以与溴水反应而使其褪色 |
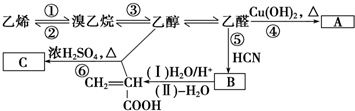
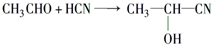 ;加成反应.
;加成反应.