题目内容
14.室温下,分别用0.1mol•L-1下列溶液进行实验,结论不正确的是( )| A. | 向CH3COONa溶液中加入盐酸至pH=7:c(Na+)=c(Cl-)+c(CH3COO-) | |
| B. | 向NaHCO3中滴入NaOH溶液至反应完全:c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)] | |
| C. | 向氨水中加入少量NH4Cl固体:$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| D. | 向NaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH=13 |
分析 A.pH=7,则c(H+)=c(OH-),则根据醋酸钠的溶液中的电荷守恒判断;
B.反应完全时恰好生成碳酸钠,根据碳酸钠溶液中的物料守恒判断;
C.铵根离子浓度增大,一水合氨的电离程度减小,溶液中氢氧根离子浓度减小,结合$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{{K}_{b}}{c(O{H}^{-})}$判断;
D.等体积、浓度为0.1mol/L的两溶液混合后,溶液呈碱性,计算出混合液中氢氧根离子浓度,然后假设混合液的pH.
解答 解:A.向CH3COONa溶液中加入盐酸至pH=7,则c(H+)=c(OH-),根据电荷守恒可知:c(Na+)=c(Cl-)+c(CH3COO-),故A正确;
B.向NaHCO3中滴入NaOH溶液至反应完全,反应后溶质为碳酸钠,根据碳酸钠溶液中的物料守恒可得:c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)],故B正确;
C.根据一水合氨的电离平衡常数可知:$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{{K}_{b}}{c(O{H}^{-})}$,向氨水中加入少量NH4Cl固体后,溶液中氢氧根离子浓度减小,则氢氧根离子浓度减小,$\frac{{K}_{b}}{c(O{H}^{-})}$=$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的比值增大,故C正确;
D.向NaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液,混合液中氢氧根离子过量,氢氧根离子浓度为:$\frac{0.1mol/L×2-0.1mol/L}{2}$=0.05mol/L,而pH=13的溶液中氢氧根离子浓度为0.1mol/L,故D错误;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒的含义为解答关键,注意掌握弱电解质电离及其影响、溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及灵活应用能力.

| A. | 乳酸薄荷醇酯( 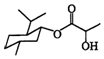 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛( 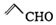 )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖 | |
| D. | CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示二者均有三种不同的氢原子且三种氢原子数的比例相同,故不能用1H-NMR来鉴别 |
| A. | 5:2 | B. | 3:1 | C. | 6:5 | D. | 1:3 |
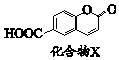
| A. | X分子式是C10H6O4 | |
| B. | X分子中有两种含氧官能团 | |
| C. | 加热条件下1 mol X最多能与2molNaOH反应 | |
| D. | 一定条件下能发生加成、水解、氧化、取代反应 |
| A. | 羟基电子式: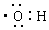 | B. | 甲醛的结构式: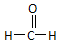 | ||
| C. | 乙醇的结构简式:CH3CH2OH | D. | 1,3-丁二烯的分子式:C4H8 |
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 氢气 | 加热 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 苯(甲苯) | 蒸馏水 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
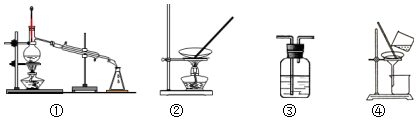
| A. | 用浓硫酸干燥SO2,选③ | |
| B. | 从食盐溶液中获取NaCl,选② | |
| C. | 除去自来水中的Cl-,制纯净水,选④和① | |
| D. | 除去Fe(OH)3胶体中的难溶物,选④ |
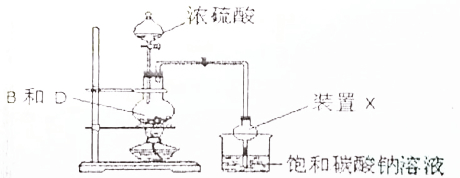
| A. | 反应中浓硫酸的作用是催化剂、吸水剂 | |
| B. | 饱和碳酸钠溶液可用饱和氢氧化钠溶液代替 | |
| C. | 实验结束后烧杯中的溶液经震荡、静置、分液,能得到纯净的乙酸乙酯 | |
| D. | 装置X的作用能防止倒吸 |