题目内容
20.下列分子的立体结构,其中属于直线型分子的是( )| A. | CH≡CH | B. | H2O | C. | P4 | D. | CH4 |
分析 根据价电子对互斥理论,价层电子对个数=σ键个数+孤电子对个数.
价层电子对个数为4,不含孤电子对,为正四面体结构;含有一个孤电子对,空间构型为三角锥形,含有两个孤电子对,空间构型是V型;
价层电子对个数为3,不含孤电子对,平面形结构;含有一个孤电子对,空间构型为为V形结构;
价层电子对个数是2且不含孤电子对,为直线形结构,据此判断.
解答 解:A.CH≡CH分子中每个C原子含有2个σ键和2个π键,价层电子对个数是2,中心原子上没有孤对电子,则分子空间构型是直线型,故A正确;
B.水分子中价层电子对个数=2+$\frac{1}{2}$×(6-2×1)=4,含有2个孤电子对,略去孤电子对后,实际上其空间构型是V型,故B错误;
C.白磷P4的结构式为 ,P原子最外层电子数是5,每个P原子形成3个共价键,P4属于正四面体结构,故C错误;
,P原子最外层电子数是5,每个P原子形成3个共价键,P4属于正四面体结构,故C错误;
D.CH4分子的中心原子C原子上含有4个σ 键,中心原子上的孤电子对数=$\frac{1}{2}$(0-4×1)=0,中心原子上没有孤对电子,所以其空间构型是正四面体结构,故D错误;
故选A.
点评 本题考查了分子的立体构型的判断,注意杂化轨道理论的理解应用,把握常见分子中原子的杂化及空间构型为解答的关键,注意孤电子对个数的计算方法,为易错点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.提纯下列物质(括号内是杂质)所用试剂和操作不正确的是( )
| A. | CO2(HCl):用NaHCO3饱和溶液洗气 | |
| B. | 植物油(水):萃取 | |
| C. | NaOH溶液(Na2CO3):加入适量的Ca(OH)2溶液 | |
| D. | Cu粉(Fe粉):加入足量稀硫酸溶液后过滤 |
11.下列离子在水溶液中能大量共存的是( )
| A. | NH4+、CH3COO-、Cl-、NO3- | B. | Ba2+、Al3+、HCO3-、NO3- | ||
| C. | Fe2+、H+、S2O32-、NO3- | D. | Na+、Al3+、AlO2-、SO42- |
8.“分子机器设计和合成”有着巨大的研究潜力.人类步入分子器件时代后,使得光控、温控和电控分子的能力更强,如图是蒽醌套索醚电控开关.下列说法错误的是( )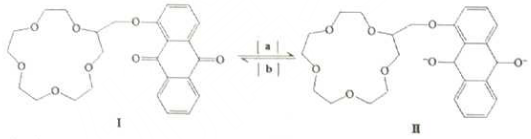

| A. | 物质Ⅰ的分子式是C25H28O8 | B. | 反应[a]是氧化反应 | ||
| C. | 1molⅠ可与8molH2发生加成反应 | D. | 物质Ⅰ的所有原子不可能共平面 |
15.下列反应的离子方程式正确的是( )
| A. | Cu(OH)2与盐酸反应:OH-+H+=H2O | |
| B. | 氯气通入HI溶液中:Cl2+I-=Cl-+I2 | |
| C. | 在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O | |
| D. | 稀H2SO4与Ba(OH)2溶液反应:Ba2++SO42-=BaSO4↓ |
5.下列说法正确的是( )
| A. | 用溴水鉴别苯和正己烷 | |
| B. | 煤气的主要成分是丁烷 | |
| C. | 石油是混合物,其分馏产品汽油为纯净物 | |
| D. | 石油催化裂化的主要目的是提高汽油等轻质油的产量与质量,石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
12.NA为阿伏伽德罗常数,下列叙述错误的是( )
| A. | 20g D2O中含的质子数为10NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 常温下,22.4L CO2气体的分子总数小于NA |
9.下列有关物质的性质与用途具有对应关系的是( )
| A. | 铝具有良好导热性,可用铝罐贮运浓硝酸 | |
| B. | 水玻璃能与酸反应,可用作生产黏合剂和防火剂 | |
| C. | NaNO2具有碱性,可用于使铁零件表面生成Fe3O4 | |
| D. | FeCl3溶液能与Cu反应,可用作铜制线路板的蚀刻剂 |