题目内容
12.下列说法正确的是( )| A. | 棉花和蚕丝的主要成分都是纤维素 | |
| B. | 淀粉和蛋白质在一定条件下都能发生水解反应生成葡萄糖 | |
| C. | 食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物 | |
| D. | 由青蒿素(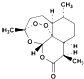 )合成双氢青蒿素( )合成双氢青蒿素(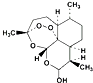 )的反应属于加成反应 )的反应属于加成反应 |
分析 A.棉花的主要成分是纤维素;蚕丝的主要成分是蛋白质;
B.蛋白质是由氨基酸组成的;
C.高分子化合物的相对分子质量特别大,一般达1万以上、一般具有重复结构单元;
D.羰基能与氢气发生加成反应.
解答 解:A.蚕丝的主要成分是蛋白质,故A错误;
B.蛋白质是由氨基酸组成的,水解最终生成氨基酸,故B错误;
C.油脂相对分子质量较小,不是高分子化合物,故C错误;
D.青蒿素含有羰基,羰基能与氢气发生加成反应,故D正确.
故选D.
点评 本题考查了生活中常见的有机物的结构和性质以及高分子化合物等知识,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
2.下列反应中,盐酸既表现出酸性又表现出氧化性的是( )
| A. | 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O | |
| B. | 2HCl$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | |
| C. | HCl+AgNO3═AgCl↓+HNO3 | |
| D. | Zn+2HCl═ZnCl2+H2↑ |
3.根据反应
①Fe+Cu2+═Fe2++Cu
②2Fe3++Cu═Cu2++2Fe2+;
③2Fe2++Cl2═2Fe3++2Cl-
④HClO+H++Cl-═Cl2+H2O
可以判断出各微粒的氧化性由强到弱的顺序正确的是( )
①Fe+Cu2+═Fe2++Cu
②2Fe3++Cu═Cu2++2Fe2+;
③2Fe2++Cl2═2Fe3++2Cl-
④HClO+H++Cl-═Cl2+H2O
可以判断出各微粒的氧化性由强到弱的顺序正确的是( )
| A. | HClO>Cl2>Fe3+>Cu2+>Fe2+ | B. | Cl2>HClO>Fe3+>Cu2+>Fe2+ | ||
| C. | Cl2>Fe3+>HClO>Cu2+>Fe2+ | D. | HClO>Cl2>Cu2+>Fe3+>Fe2+. |
20.下列说法或表示方法正确的是( )
| A. | 甲烷的标准燃烧热为-890.3 kJ•molˉ1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•molˉ1 | |
| B. | 由C(石墨,s)=C(金刚石,s)△H=+1.9 kJ•molˉ1可知,金刚石比石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OHˉ(aq)=H2O(l)△H=-57.3 kJ•molˉ1,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ | |
| D. | 一定条件下,某密闭容器中充入2 mol SO2(g)和1 mol O2(g),达到平衡后,放出Q kJ热量,则该条件下的热化学方程式为:2SO2(g)+O2(g)?2SO3(g )△H=-Q kJ•molˉ1 |
7.下列各表述与示意图一致的是( )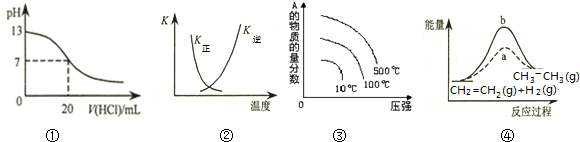

| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)═2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 | |
| C. | 对于可逆反应:A2(g)+3B2(g)?2AB3(g)△H>0,图③表示的是压强、温度、A的物质的量的分数的关系 | |
| D. | 图④中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
2.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g•L-1;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X>M | |
| B. | YZ2溶于水形成的溶液具有较强的氧化性 | |
| C. | 1molWM溶于足量水中完全反应共转移2mol电子 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
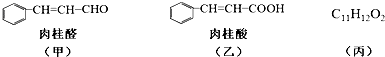
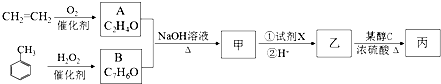
 .
. $→_{△}^{氢氧化钠溶液}$
$→_{△}^{氢氧化钠溶液}$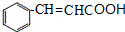 +H2O.
+H2O.