题目内容
18.下列微粒中,跟NH4+的电子总数和质子总数相同的是( )| A. | Ne | B. | F | C. | H3O+ | D. | CH4 |
分析 由于N的质子数为7,H的质子数为1,所以NH4+中质子数为11,电子数为10个.对于电中性原子:质子数=电子数,阳离子:质子数-所带电荷数目=电子数;阴离子:质子数+所带电荷数目=电子数.
解答 解:A.Ne中质子数为10,电子数为10,故A错误;
B.F-中质子数为9,电子数为10个,故B错误;
C.H3O+中质子数为11,电子数为10,故C正确;
D.CH4中质子数为10,电子数为10,故D错误.
故选C.
点评 本题考查微粒质子数、电子数的相互关系,难度较小,关键理解质子数与电子数关系确定微粒电性.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
8.我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务.下列有关海水综合利用的说法不正确的是( )
| A. | 从海水中提炼出的氘(含HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题,成为一条新的科学思路,HDO与H2O化学性质相同 | |
| B. | 从海水中提取镁可以采用下列方法:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液→MgCl2•6H2O$\stackrel{HCl}{→}$MgCl2 (熔融)$\stackrel{电解}{→}$Mg | |
| C. | 从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,在该化合物中,碘元素呈+3和+5两种价态,这种化合物的化学式是I4O9 | |
| D. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
6.NA表示阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 常温常压下,16g O3所含的原子数为NA | |
| B. | 标准状况下,11.2 L NO和11.2 L O2混合后气体的分子总数为NA | |
| C. | 常温下,pH=2的稀盐酸中所含有的H+离子数等于0.01 NA | |
| D. | 加热条件下,20mL 10 mol/L 浓硝酸与足量铜反应转移电子数等于0.2NA |
13.下列四种固体物质中,既存在离子键又存在共价键的是( )
| A. | NH4Cl | B. | HCl | C. | MgCl2 | D. | CH4 |
3.下列化合物中,既能发生水解反应,又能发生消去反应,且消去反应生成的烯烃不存在同分异构体的是( )
| A. | CH3Cl | B. | 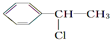 | C. | 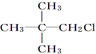 | D. | 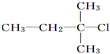 |
10.下列说法正确的是( )
| A. | 向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中水的电离程度始终增大 | |
| B. | 0.01mol•L-1CH3COOH溶液中水的电离程度小于0.01mol•L-1盐酸中水的电离程度 | |
| C. | 将0.01mol•L-1盐酸与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)<1×10-7mol•L-1 | |
| D. | 将0.01mol•L-1的CH3COOH溶液与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)>1×10-7mol•L-1 |
7.下列有关溶液中粒子浓度的比较中不正确的是( )
| A. | 饱和氯水中滴加0.1mol/L的NaOH溶液:c(H+)+c(Na+ )=2c(ClO-)+c(HClO)+c(OH-) | |
| B. | 向20mL 0.2mol/L 的H2S溶液中逐滴加入0.2mol/L的NaOH溶液30mL,溶液中存在以下关系:c(S2-)+2c(OH-)=c(HS-)+2c(H+)+2c(H2S) | |
| C. | pH相同的①CH3COONa②NaClO 二种溶液的c(Na+):①>② | |
| D. | 常温下,向20mL 0.1mol/L的CH3COONa溶液中逐滴加入0.1mol/L盐酸溶液的pH=7时,c(CH3COOH)=c(Cl-)>c(OH-)=c(H+) |
10.下列烷烃的系统命名中,正确的是( )
| A. | 2-甲基丙烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 3-甲基-2-乙基戊烷 | D. | 2,3,3-三甲基丁烷 |