题目内容
18.下列说法正确的是( )| A. | 随原子序数递增,ⅦA族元素的最高价氧化物对应水化物酸性逐渐增强 | |
| B. | 第三周期元素中(除稀有气体元素)简单离子半径最小的元素,其氧化物具有两性 | |
| C. | 第三周期气态氢化物的沸点均为同主族中沸点最低 | |
| D. | 第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大 |
分析 A.元素的非金属越强,其最高价氧化物的水化物酸性越强,但F、O元素除外;
B.第三周期中,离子半径先减小后增大再减小,离子半径最小的是铝离子,氧化铝属于两性氧化物;
C.氢化物的熔沸点与分子间作用力和氢键有关,含有氢键的氢化物熔沸点较高;
D.同一周期元素,元素的最高正化合价与其族序数相等但除F、O元素外.
解答 解:A.元素的非金属越强,其最高价氧化物的水化物酸性越强,但F、O元素除外,第VIIA族元素,其非金属性随着原子序数增大而减弱,但F没有最高价氧化物的水化物,则从Cl到At元素,其最高价氧化物的水化物酸性逐渐减弱,故A错误;
B.第三周期中,离子半径先减小后增大再减小,离子半径最小的是铝离子,氧化铝属于两性氧化物,能溶于强酸和强碱溶液,故B正确;
C.氢化物的熔沸点与分子间作用力和氢键有关,含有氢键的氢化物熔沸点较高,甲烷中不含氢键,所以硅烷的熔沸点高于甲烷,故C错误;
D.同一周期元素,元素的最高正化合价与其族序数相等但除F、O元素外,所以第二周期中除了F、O元素外,元素最高正化合价随着原子序数增大而增大,故D错误;
故选B.
点评 本题考查元素周期律,为高频考点,侧重考查学生分析判断及知识运用能力,注意规律中的反常现象,熟练掌握元素周期律并灵活运用,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
19.苯环结构中不存在碳碳单、双键交替出现的结构,下列可以作为证据的事实是( )
①苯不能使高锰酸钾酸性溶液褪色 ②苯不能使溴水因发生化学反应而褪色
③苯在加热和有催化剂存在的条件下能生成环己烷 ④苯中碳碳键长完全相等
⑤邻二氯苯只有一种 ⑥间二氯苯只有一种.
①苯不能使高锰酸钾酸性溶液褪色 ②苯不能使溴水因发生化学反应而褪色
③苯在加热和有催化剂存在的条件下能生成环己烷 ④苯中碳碳键长完全相等
⑤邻二氯苯只有一种 ⑥间二氯苯只有一种.
| A. | ①②④⑤ | B. | ①②③④⑥ | C. | ①⑤ | D. | ①② |
6.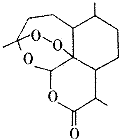 2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
 2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )
2015年10月5日,中国科学家屠哟坳首次获诺贝尔生理学或医学奖,以表彰她创制新型抗疟药-青蒿素和双氢青蒿素,其中青蒿素的结构简式如图所示,则青蒿素分子中碳、氧原子的个数比为( )| A. | 2:1 | B. | 3:1 | C. | 12:5 | D. | 16:5 |
13.下列各组有机物不管它们以任何比例混合,只要混合物的物质的量一定,则在完全燃烧时消耗氧气的量恒定不变的是( )
| A. | C3H6和C3H8 | B. | C4H6和C3H8 | C. | C5H12和C6H6 | D. | C3H6和C3H8O |
3.已知铍元素是第二周期第ⅡA族元素,化学性质与铝相似,下列叙述正确的是( )
| A. | 常温下,单质铍能与水反应放出H2 | |
| B. | Be(OH)2易溶于水 | |
| C. | Be(OH)2溶于盐酸,也可能溶于NaOH溶液 | |
| D. | BeCl2中各原子中的最外层电子层都满足8电子结构 |
7.下列现象与形成配合物无关的是( )
| A. | 向FeCl3中滴入KSCN,出现红色 | |
| B. | 向Cu与Cl2反应后的集气瓶中加少量H2O,呈绿色,再加水,呈蓝色 | |
| C. | Cu与浓硝酸反应后,溶液呈绿色;Cu与稀硝酸反应后,溶液呈蓝色 | |
| D. | 向AlCl3中逐滴滴加NaOH至过量,先出现白色沉淀,继而消失 |
8.从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4下列说法正确的是( )
| A. | Cu2S是还原产物,反应中1 mol CuSO4失1 mol电子 | |
| B. | 5 mol FeS2发生反应,有10 mol电子转移 | |
| C. | 产物中的SO42-离子有一部分是氧化产物 | |
| D. | FeS2只作还原剂 |