题目内容
目前有科学家在一定条件下利用水煤气(CO+H2)合成甲醇:CO(g)+2H2(g)
CH3OH(g),甲醇的物质的量与反应温度的关系如图所1示:
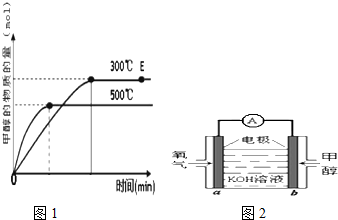
①合成甲醇反应的△H 0.(填“>”、“<”或“=”)
②其它条件不变,将E点的容积压缩到原来的
,正反应速率加快,逆反应速率 .(填“加快”、“减慢”、“不变”),重新平衡时
.(填“增大”、“减小”或“不变”)
③230℃时,平衡常数K=1.若其它条件不变,将温度升高到450℃时,达到平衡时,K 1.(填“>、<或=”)
④利用甲醇燃料电池设计如图2所示的装置:写出b极的电极反应式 .
| Cu2O/ZnO |

①合成甲醇反应的△H
②其它条件不变,将E点的容积压缩到原来的
| 1 |
| 2 |
| c(CH3OH) |
| c(CO) |
③230℃时,平衡常数K=1.若其它条件不变,将温度升高到450℃时,达到平衡时,K
④利用甲醇燃料电池设计如图2所示的装置:写出b极的电极反应式
考点:化学平衡的影响因素,化学电源新型电池
专题:化学平衡专题,电化学专题
分析:①由甲醇的物质的量与反应温度的关系图可知温度越高甲醇的物质的量越低来判断水煤气合成甲醇的反应热;
②由容积压缩则压强增大,利用压强对化学反应速率及化学平衡的影响来分析;
③根据温度对化学平衡的影响来分析化学平衡常数的变化;
④写出甲醇燃料电池在碱性环境中的正极反应式和总反应式,利用正极反应式+负极反应式=总反应式,写出负极反应式.
②由容积压缩则压强增大,利用压强对化学反应速率及化学平衡的影响来分析;
③根据温度对化学平衡的影响来分析化学平衡常数的变化;
④写出甲醇燃料电池在碱性环境中的正极反应式和总反应式,利用正极反应式+负极反应式=总反应式,写出负极反应式.
解答:
解:①由图可知,500℃比300℃达平衡时甲醇的物质的量小,即升高温度化学平衡逆向移动,则正反应为放热反应,△H<0,故答案为:<;
②由其它条件不变,将E点的容积压缩到原来的1/2,则容积压缩时压强增大,加压时正、逆反应速率都加快,由水煤气合成甲醇的反应可知,
该反应是气体体积缩小的反应,则加压时平衡正向移动,甲醇的物质的量增大,CO的物质的量减小,则c(CH3OH)/c(CO)增大,
故答案为:加快;增大;
③由230℃时,平衡常数K=1,该反应为放热反应,由K=
,温度升高到450℃时平衡向逆反应方向移动,生成物的浓度变小,
则K<1,故答案为:<;
(3)因有机物能使蛋白质变性,故A 说法正确;甲醇中没有邻位碳原子,则不能发生消去反应,故B说法错误;
由甲醇中碳原子连接羟基和氢原子,则能被氧化,故C说法错误;由甲醇中的羟基氢不如水中的羟基氢活泼,则甲醇与钠反应不如水与钠反应剧烈,
故答案为:A;
(4)在碱性环境中,总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,由图可知,甲醇燃料电池中a极通入氧气,在碱性条件氧气得电子生成氢氧根离子,即通入氧气的为正极,正极反应为O2+4e-+2H2O-═4OH-,总反应式-正极反应式,去掉氧气,可得b的负极反应式为:CH3OH+8OH--6e-=CO32-+6H2O,
故答案为:CH3OH+8OH--6e-=CO32-+6H2O.
②由其它条件不变,将E点的容积压缩到原来的1/2,则容积压缩时压强增大,加压时正、逆反应速率都加快,由水煤气合成甲醇的反应可知,
该反应是气体体积缩小的反应,则加压时平衡正向移动,甲醇的物质的量增大,CO的物质的量减小,则c(CH3OH)/c(CO)增大,
故答案为:加快;增大;
③由230℃时,平衡常数K=1,该反应为放热反应,由K=
| 生成物浓度幂之积 |
| 反应物浓度幂之积 |
则K<1,故答案为:<;
(3)因有机物能使蛋白质变性,故A 说法正确;甲醇中没有邻位碳原子,则不能发生消去反应,故B说法错误;
由甲醇中碳原子连接羟基和氢原子,则能被氧化,故C说法错误;由甲醇中的羟基氢不如水中的羟基氢活泼,则甲醇与钠反应不如水与钠反应剧烈,
故答案为:A;
(4)在碱性环境中,总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,由图可知,甲醇燃料电池中a极通入氧气,在碱性条件氧气得电子生成氢氧根离子,即通入氧气的为正极,正极反应为O2+4e-+2H2O-═4OH-,总反应式-正极反应式,去掉氧气,可得b的负极反应式为:CH3OH+8OH--6e-=CO32-+6H2O,
故答案为:CH3OH+8OH--6e-=CO32-+6H2O.
点评:本题考查知识点较多,综合性强,注重对基础知识和基本技能的考查,同时注重对高考热点的训练,明确热化学方程式、化学平衡、化学反应速率、电化学等重要知识点是解答的关键.

练习册系列答案
相关题目
1999年度诺贝尔化学奖授予了开创“飞秒(10-15s)化学”新领域的科学家,使运用激光光谱技术观测化学反应时分子中原子运动成为可能.你认为该技术不能观察到的是( )
| A、原子中原子核的内部结构 |
| B、化学反应中原子的运动 |
| C、化学反应中生成物分子的形成 |
| D、化学反应中反应物分子的分解 |
金属卤化物跟卤素化合可生成多卤化物,如:KI+I2?KI3,有关KI3的叙述中不正确的是( )
| A、I2在KI溶液中溶解度增大是由于生成I3-离子 |
| B、I3-在溶液中存在下列平衡I3-?I2+I- |
| C、KI3溶液遇淀粉不变蓝色 |
| D、将Cl2通入KI3溶液中,I3-浓度减小 |
 组成蛋白质的元素主要有C、H、O、N及S、P和少量的Zn、Cu等.
组成蛋白质的元素主要有C、H、O、N及S、P和少量的Zn、Cu等.
 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示. 如图所示的装置中,甲为铜锌原电池,A、B均为石墨电极.回答下列问题:
如图所示的装置中,甲为铜锌原电池,A、B均为石墨电极.回答下列问题: