题目内容
下列框图中的物质中B、C、D为单质,其余为化合物(或其水溶液)
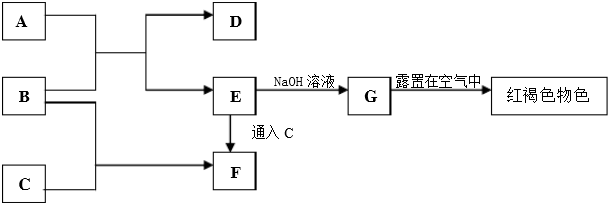
已知A与AgNO3反应生成白色沉淀,C与D反应后的物质溶于水得到A,试回答下列问题:
(1)框图转化中,发生的氧化还原反应有 个(用A、B、C等回答)
A.2 B.3 C.4 D.5
(2)写出下列物质的化学式:A物质 B物质 C物质
(3)G到H的转化过程中有关的现象 ,有关的化学方程式是 .
(4)E中通入C,可以得到F,写出溶液中发生离子反应的方程式 检验F溶液中的金属阳离子常用的方法和现象是 .

已知A与AgNO3反应生成白色沉淀,C与D反应后的物质溶于水得到A,试回答下列问题:
(1)框图转化中,发生的氧化还原反应有
A.2 B.3 C.4 D.5
(2)写出下列物质的化学式:A物质
(3)G到H的转化过程中有关的现象
(4)E中通入C,可以得到F,写出溶液中发生离子反应的方程式
考点:无机物的推断
专题:推断题
分析:G在空气中生成红褪色物质,是氢氧化亚铁被氧气氧化成氢氧化铁,所以G为氢氧化亚铁,推知E为亚铁盐,B、D为单质,A+B→E+D,该反应为置换反应也是氧化还原反应,且A与AgNO3反应生成白色沉淀,可推知A为盐酸,B为铁,D为氢气,E为氯化亚铁,C与D反应后的物质溶于水得到A,所以C为氯气,氯化亚铁溶液中通入氯气发生氧化反应得氯化铁,B与C的反应为铁与氯气发生氧化还原反应生成氯化铁,据此答题.
解答:
解:G在空气中生成红褪色物质,是氢氧化亚铁被氧气氧化成氢氧化铁,所以G为氢氧化亚铁,推知E为亚铁盐,B、D为单质,A+B→E+D,该反应为置换反应也是氧化还原反应,且A与AgNO3反应生成白色沉淀,可推知A为盐酸,B为铁,D为氢气,E为氯化亚铁,C与D反应后的物质溶于水得到A,所以C为氯气,氯化亚铁溶液中通入氯气发生氧化反应得氯化铁,B与C的反应为铁与氯气发生氧化还原反应生成氯化铁,
(1)框图转化中,发生的氧化还原反应有4个,故选C;
(2)A物质的化学式为盐酸(HCl),B物质的化学式为 Fe,C物质的化学式为Cl2,故答案为:盐酸(HCl);Fe;Cl2;
(3)G到H的转化是氢氧化亚铁被氧化的过程,有关的现象是白色迅速变为灰绿色,最后变为红褐色,有关的化学方程式是4 Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白色迅速变为灰绿色,最后变为红褐色;4 Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)氯气通入氯化亚铁溶液中发生离子反应的方程式为2Fe2++Cl2=2Fe3++2Cl-,检验氯化铁溶液中的铁离子常用的方法和现象是滴加少许KSCN溶液若立即出现红色即可证明的Fe3+存在,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;滴加少许KSCN溶液若立即出现红色即可证明的Fe3+存在.
(1)框图转化中,发生的氧化还原反应有4个,故选C;
(2)A物质的化学式为盐酸(HCl),B物质的化学式为 Fe,C物质的化学式为Cl2,故答案为:盐酸(HCl);Fe;Cl2;
(3)G到H的转化是氢氧化亚铁被氧化的过程,有关的现象是白色迅速变为灰绿色,最后变为红褐色,有关的化学方程式是4 Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白色迅速变为灰绿色,最后变为红褐色;4 Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)氯气通入氯化亚铁溶液中发生离子反应的方程式为2Fe2++Cl2=2Fe3++2Cl-,检验氯化铁溶液中的铁离子常用的方法和现象是滴加少许KSCN溶液若立即出现红色即可证明的Fe3+存在,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;滴加少许KSCN溶液若立即出现红色即可证明的Fe3+存在.
点评:本题以框图题形式考查无机物的推断、物质之间的转化关系等,题目难度不大,红褪色物质为推断的突破口,注意基础知识的掌握.

练习册系列答案
相关题目
在实验室中,下列试剂不需要用棕色试剂瓶保存的是( )
| A、氯水 | B、硝酸银 |
| C、浓硝酸 | D、漂白粉 |
现需要480ml 0.1mol/L-1NaOH溶液,需选取500mL容量瓶进行配制,以下操作正确的是( )
| A、称取2.0gNaOH,加入480ml水 |
| B、称取2.0gNaOH,配制480mL溶液 |
| C、称取2.0gNaOH,加入500mL水 |
| D、称取2.0gNaOH,配制500mL溶液 |
下列溶液中有关物质的量浓度关系不正确的( )
| A、pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) |
| B、0.1mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(A2-)>c(H2A) |
| C、物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
| D、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |

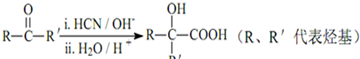
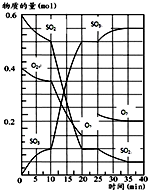 500℃时,将SO2和O2置于一容积固定为2L的密闭容器中发生反应,反应过程中SO2、O2和SO3物质的量变化如图所示.
500℃时,将SO2和O2置于一容积固定为2L的密闭容器中发生反应,反应过程中SO2、O2和SO3物质的量变化如图所示.