题目内容
下列各现象不能用平衡移动原理解释的是( )
| A、FeS 不溶于水,但能溶于稀盐酸中 |
| B、CaCO3难溶于稀硫酸中,却能溶于醋酸中 |
| C、分别用等体积的蒸馏水和稀硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸造成的损失量 |
| D、Cl2 与 Na2S 溶液反应生成单质 S 沉淀 |
考点:化学平衡移动原理
专题:
分析:平衡移动原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,平衡移动原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用平衡移动原理解释.
解答:
解:A.FeS在水溶液中存在溶解平衡FeS(s)?Fe2++S2-,S2-和H+反应生成弱电解质H2S,从而促进FeS溶解,所以可以用平衡移动原理解释,故A不选;
B.CaCO3在水溶液中存在溶解平衡CaCO3(s)?Ca2++CO32-,CaSO4微溶、醋酸钙易溶于水,所以醋酸促进碳酸钙分解,可以用平衡移动原理解释,故B不选;
C.BaSO4在水溶液中存在溶解平衡BaSO4(s)?Ba2++SO42-,向溶液中加入稀硫酸,硫酸根离子浓度增大而抑制硫酸钡溶解,所以可以用平衡移动原理解释,故C不选;
D.Cl2与Na2S发生氧化还原生成S沉淀且Na2S在水溶液中不存在溶解平衡,所以不能用平衡移动原理解释,故D选;
故选D.
B.CaCO3在水溶液中存在溶解平衡CaCO3(s)?Ca2++CO32-,CaSO4微溶、醋酸钙易溶于水,所以醋酸促进碳酸钙分解,可以用平衡移动原理解释,故B不选;
C.BaSO4在水溶液中存在溶解平衡BaSO4(s)?Ba2++SO42-,向溶液中加入稀硫酸,硫酸根离子浓度增大而抑制硫酸钡溶解,所以可以用平衡移动原理解释,故C不选;
D.Cl2与Na2S发生氧化还原生成S沉淀且Na2S在水溶液中不存在溶解平衡,所以不能用平衡移动原理解释,故D选;
故选D.
点评:本题考查化学平衡移动原理,侧重考查原理应用,明确原理内涵即可解答,知道难溶物溶解、弱电解质电离、盐类水解中都存在平衡,平衡移动原理适用于可逆反应,不能用于不可逆反应.

练习册系列答案
相关题目
100mL浓度为2mol?L-1的盐酸溶液跟过量的锌片反应,为减慢反应速率,又不影响生成H2的总量,可采用的方法有( )
| A、加适量6mol?L-1HCl溶液 |
| B、加数滴CuCl2溶液 |
| C、加适量醋酸钠固体 |
| D、加适量NaNO3溶液 |
氢化铝钠(NaAlH4)是最有研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4
Na3AlH6+2Al+3H2↑.下列说法正确的是( )
| ||
| A、NaAlH4中含有离子键和非极性共价键 |
| B、每生成11.2 L(标准状况下)H2,转移NA个电子 |
| C、NaAlH4中氢元素为+1价,在反应中有50%的氢被还原 |
| D、反应中氧化产物与还原产物的物质的量之比为1:1 |
“纳米材料”是直径从几纳米至几十纳米的材料.如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是( )
| A、所得分散系极不稳定 |
| B、具有丁达尔效应 |
| C、不能透过滤纸 |
| D、以上性质都不具有 |
水的电离平衡曲线如图所示,下列说法不 正确的是( )
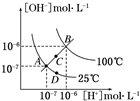

| A、图中四点KW间的关系:A=D<C<B |
| B、若从A点到C点,可采用温度不变在水中加少量CH3COONa固体 |
| C、若从A点到D点,可采用温度不变在水中加少量酸 |
| D、若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性 |
 的正确命名是( )
的正确命名是( )| A、2,2-二乙基丁烷 |
| B、3-甲基-2-乙基戊烷 |
| C、2-乙基-3甲基-戊烷 |
| D、3,4-二甲基己烷 |
 (1)火力发电厂时燃煤排烟中含有大量的氢氧化物(NOx),可利用甲烷和NOx在一定条件下反应消除其污染,写出CH4与NO2反应的化学方程式
(1)火力发电厂时燃煤排烟中含有大量的氢氧化物(NOx),可利用甲烷和NOx在一定条件下反应消除其污染,写出CH4与NO2反应的化学方程式