题目内容
3.取7.65g Al2O3溶于300mL 2mol/L 盐酸溶液中,待充分反应后,再逐滴加入2mol/L NaOH溶液.试回答:(1)当加入75mL NaOH溶液时,开始出现沉淀.
(2)当加入到300 mL NaOH溶液时,沉淀量达到最大值,其沉淀质量为11.7g.
分析 取7.65g Al2O3的物质的量为:$\frac{7.65g}{102g/mol}$=0.075mol,300mL 2mol/L 盐酸溶液的物质的量为:0.3×2mol=0.6mol,由Al2O3~6HCl可知,0.075mol的氧化铝消耗盐酸的物质的量为0.45mol,所以过量的盐酸的物质的量为:0.6-0.45=0.15mol,所以氢氧化钠首先与过量和盐酸反应,由此分析解答.
解答 解:取7.65g Al2O3的物质的量为:$\frac{7.65g}{102g/mol}$=0.075mol,300mL 2mol/L 盐酸溶液的物质的量为:0.3×2mol=0.6mol,由Al2O3~6HCl可知,0.075mol的氧化铝消耗盐酸的物质的量为0.45mol,所以过量的盐酸的物质的量为:0.6-0.45=0.15mol,所以氢氧化钠首先与过量和盐酸反应,
(1)盐酸消耗氢氧化钠的物质的量为:$\frac{0.15}{2}$=0.075L=75mL,故答案为:75;
(2)沉淀量达到最大值消耗氢氧化钠的体积为:75mL+$\frac{0.075mol×2×3}{2mol/L}×1000ml/L$=300mL,其沉淀质量为0.075mol×2×78g/mol=11.7g,
故答案为:300mL;11.7g.
点评 本题考查化学计算,涉及方程式的计算、混合物的计算、图象计算等,难度中等,清楚图象各段反应是解题的关键.

练习册系列答案
相关题目
13.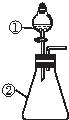 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选項 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 氢氧化钠稀溶液 | 硫酸铝铵溶液 | 立即产生白色沉淀 |
| B | 氢氧化钠浓溶液 | 用砂纸打磨过的镁条 | 立即产生大量无色气体 |
| C | 浓硫酸 | 铜粉 | 立即产生刺激性气味气体 |
| D | 盐酸 | 较浓的硝酸亚铁溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
14.已知阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1 mol/L CuCl2溶液中含有的Cl-的个数为2NA | |
| B. | 16 g甲烷中含有的共用电子对数为NA | |
| C. | 常温常压,46 gNO2与N2O4的混合气体中含有的原子数为3NA | |
| D. | 4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
11.已知短周期元素的离子,A2+、B+、C2-、D-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | B. | 原子序数 D>C>B>A | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
18.下列仪器中没有“0”刻度线的是( )
| A. | 托盘天平的游码刻度尺 | B. | 温度计 | ||
| C. | 酸式滴定管 | D. | 量筒 |
15.某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录(按编号填写):
实验结论:
Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:A E F.(多选)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录(按编号填写):
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | ① | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | / | Zn+Fe2+=Zn2++Fe | ② |
| ③ | 在FeCl3溶液中加入足量铁粉 | ③ | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | ④ | / | / | Fe3+具有氧化性 |
Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:A E F.(多选)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
12.用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 12.0g熔融的NaHSO4中含有的阳离子数为0.1NA | |
| B. | 2mol SO2和1mol O2在一定条件下充分反应后,所得混合气体的分子数大于2NA | |
| C. | 常温下,5.6g Fe片投入到足量的浓硝酸中,转移电子数为0.3NA | |
| D. | 常温常压下,14g乙烯和丙烯的混合气体中含有的原子总数为3NA |
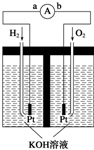 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: