��Ŀ����
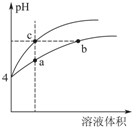
3��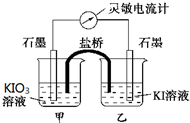 ����ӦIO3-+5I-+6H+?3I2+3H2O��Ƴ���ͼ��ʾ��ԭ��أ��ס����ձ��ж����������Һ����ʼʱ����ձ��м�������Ũ���ᣬ������ָ�뷢��ƫת��һ��ʱ�������ָ��ص��㣬������ձ��е��뼸��ŨNaOH��Һ��������ָ���ٴη���ƫת�������жϲ���ȷ���ǣ�������
����ӦIO3-+5I-+6H+?3I2+3H2O��Ƴ���ͼ��ʾ��ԭ��أ��ס����ձ��ж����������Һ����ʼʱ����ձ��м�������Ũ���ᣬ������ָ�뷢��ƫת��һ��ʱ�������ָ��ص��㣬������ձ��е��뼸��ŨNaOH��Һ��������ָ���ٴη���ƫת�������жϲ���ȷ���ǣ�������| A�� | ���ε�����ָ��ƫת�����෴�������ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬ | |
| B�� | ����ʵ���У������е��������ƶ������෴ | |
| C�� | ��ʼ��������Ũ����ʱ��ֻ�����ձ�����Һ���� | |
| D�� | ����ձ��е��뼸��ŨNaOH��Һ������ʯī�缫�Ϸ�����ԭ��Ӧ |
���� ��ʼʱ����ձ��м�������Ũ���ᣬ����I-ʧ��������I2����Ϊ����������IO3-�õ�������I2����Ϊ���������Լ��������Һ�������ձ��о�����ɫ���÷�ӦΪ���淴Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵ�Ũ�Ȳ��ٸı䣬��û�е���ͨ�������ƣ����Ե����ƶ���Ϊ�㣬������ձ��е��뼸��ŨNaOH��Һ�����I2��ʧ��������IO3-����Ϊ��������Ϊ������ԭ����е�����������������ƶ���
��� �⣺��ʼʱ����ձ��м�������Ũ���ᣬ����I-ʧ��������I2����Ϊ����������IO3-�õ�������I2����Ϊ�������÷�ӦΪ���淴Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵ�Ũ�Ȳ��ٸı䣬��û�е���ͨ�������ƣ����Ե����ƶ���Ϊ�㣬������ձ��е��뼸��ŨNaOH��Һ�����I2��ʧ��������IO3-����Ϊ��������Ϊ������
A���÷�ӦΪ���淴Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵ�Ũ�Ȳ��ٸı䣬��û�е���ͨ�������ƣ����Ե����ƶ���Ϊ�㣬��A��ȷ��
B��ԭ����е�����������������ƶ�������ʵ����������������������ʵ���������е��������ƶ������෴����B��ȷ��
C����ʼ��������Ũ����ʱ���ס����ձ��о��еⵥ�����ɣ��������ձ��о�����ɫ����C����
D������ձ��е��뼸��ŨNaOH��Һ�����I2��ʧ��������IO3-����Ϊ��������Ϊ����������ʯī�缫�Ϸ�����ԭ��Ӧ����D��ȷ��
��ѡ��C��
���� ���⿼����ԭ���ԭ����Ӧ�ã��ؼ�����ȷ������������ԭ��Ӧ�ж�ԭ��ص�����������Ŀ�Ѷ��еȣ�

��Pb+2Cl2�TPbCl4��Sn+2Cl2�TSnCl4��SnCl2+Cl2�TSnCl4
��PbO2+4HCl�TPbCl4+2H2O��Pb3O4+8HCl�T3PbCl2+Cl2��+4H2O��
| A�� | �ڢۢ� | B�� | �ڢۢ� | C�� | �٢ڢ� | D�� | �٢ڢܢ� |
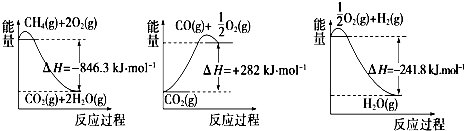
��1���ϳɰ��õ��������Լ���Ϊԭ���Ƶã�CH4��g��+H2O��g��?CO��g��+3H2��g�����йػ�ѧ��Ӧ�������仯��ͼ��ʾ��CH4��g����H2O��g����Ӧ����CO��g����H2��g�����Ȼ�ѧ����ʽΪCH4��g��+H2O��g��=CO��g��+3H2 ��g����H=+161.1kJ•mol-1��
��2��CO�Ժϳɰ��Ĵ����ж������ã��������������ͭ������Һ������ԭ������CO���䷴Ӧԭ��Ϊ[Cu��NH3��2CH3COO]��l��+CO��g��+NH3��g��?[Cu��NH3��3]CH3COO•CO��l����H��0������CO�������ͭ��Һ�����ʵ��������ֿ��������ָ�������CO�������Թ�ѭ��ʹ�ã�����������������B��������ĸ��
A�����¡���ѹ B�����¡���ѹ C�����¡���ѹ D�����¡���ѹ
��3���ð�����ȡ����[CO��NH2��2]�ķ�ӦΪ2NH3��g��+CO2��g��?CO��NH2��2��l��+H2O��g����H��0��ij�¶��£����ݻ�Ϊ100L���ܱ�������ͨ��4molNH3��2molCO2���÷�Ӧ���е�40sʱ�ﵽƽ�⣬��ʱCO2��ת����Ϊ50%�����¶��´˷�Ӧƽ�ⳣ��K��ֵΪ2500 L2•mol-2��
��4��������ʩ����������ͨ��ת��Ϊ̼��炙�̼����狀�ű����������ã����ط�����������ڵ���ø�����£�ת��Ϊ̼��泥���֪���������ˮ�еĵ���ƽ�ⳣ����25�棩��������г�����0.1mol•L-1�ģ�NH4��2CO3��Һ��
| ������� | H2CO3 | NH3•H2O |
| Ka1 | 4.30��10-7 | 1.77��10-5 |
| Ka2 | 5.61��10-11 |
�ھ���Һ������֮�������й�ϵʽ������Ϊ���в���ȷ����B��
A��c��NH4+����c��CO32-����c��HCO3-����c��NH3•H3O��
B��c��NH4+��+c��H+��=c��HCO3-��+c��OH-��+c��CO32-��
C��c��CO32-��+c��HCO3-��+c��H2CO3��=0.1mol•L-1
D��c��NH4+��+c��NH3•H2O��=2c��CO32-��+2c��HCO3-��+2c��H2CO3��

��֪�����ֽ������ӳ�����pH����ش��������⣺
| Fe2+ | Fe3+ | Cu2+ | Mn2+ | |
| ��ʼ������pH | 7.5 | 3.2 | 5.2 | 8.8 |
| ��ȫ������pH | 9.7 | 3.7 | 7.8 | 10.4 |
A���ʵ������¶� B���ʵ�����ѹǿ
C����ĥ��ʯ D���������������ˮ
��2���ܽ������з�������Ҫ��Ӧ�ǣ�FeS2��MnO2��ϡ�����з�Ӧ����Fe3+��Mn2+��SO42-��H2O���ڸ÷�Ӧ��ƽ�����ӷ���ʽ�У�������ǰ��Ļ�ѧ������Ϊ15��
��3�����������У����ȼ������̿�Ӧ�����ӷ���ʽΪ2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O��
���ټ���ʯ�ҵ�Ŀ����3.7��5.2��
��4�����������Ŀ���dz�ȥ��Һ�е�Cu2+��Ca2+�����ʣ��������Һ��c��F����=0.01mol•L-1����Һ�в���c��Ca2+��=1.5��10��6mol•L-1����Ksp��CaF2��=1.5��10��10��mol3•L-3����
��5�����̹����У�298K��c��Mn2+��Ϊ1.05mol•L-1ʱ��ʵ����MnCO3�IJ�������Һ��pH����Ӧʱ���ϵ��ͼ2��ʾ���ԱȲ�ͬ��Ӧ�����µ����ߣ�����ͼ����Ϣ�����ܻ�õĽ����У�
��pH����7.0ʱ��Ӧ������죬��MnCO3������ߣ���pHԽ��Խ����������MnCO3�IJ��ʣ�
��6������ƷA����Ҫ�ɷ��ǣ�NH4��2SO4��
| A�� | 6.5g����Zn����������ᷴӦ����������Ũϡ��ת�Ƶ�������Ϊ0.2Na | |
| B�� | ����1mol FeCl3����Һ��������������3NA | |
| C�� | ���Ե缫���ʳ��ˮ������·��ͨ��NA���ӵ�������������������11.2L | |
| D�� | Na2S��Na2O2 ��������15.6g�У����е���������Ϊ0.3NA |
 Ϊ��֤��һˮ�ϰ���NH3•H2O����������ʣ��ס��Ҷ��˷ֱ�ѡ�������Լ�����ʵ�飺��ˮ��0.10mol•L-1NH4Cl��Һ��NH4Cl���塢��̪��Һ��pH��ֽ������ˮ��
Ϊ��֤��һˮ�ϰ���NH3•H2O����������ʣ��ס��Ҷ��˷ֱ�ѡ�������Լ�����ʵ�飺��ˮ��0.10mol•L-1NH4Cl��Һ��NH4Cl���塢��̪��Һ��pH��ֽ������ˮ��