题目内容
用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉.对加入铁粉充分反应后的溶液分析合理的是( )
| A、若无固体剩余,则溶液中一定有Fe3+ |
| B、若溶液中有Cu2+,则一定没有固体析出 |
| C、若有固体存在,则溶液中一定有Fe2+ |
| D、若溶液中有Fe2+,则一定有Cu析出 |
考点:氧化还原反应的计算
专题:
分析:FeCl3溶液腐蚀印刷电路板上的铜发生反应:Cu+2Fe3+=Cu2++2Fe2+,Fe3+ 氧化性强于Cu2+,加入铁粉先与Fe3+反应,再与Cu2+反应,以此来解答.
解答:
解:A.无固体剩余,说明铜全部以铜离子形式存在,加入的铁完全反应,溶液中一定含有Fe2+,可能含有Fe3+,故A错误;
B.若溶液中有Cu2+,加入的铁量不足,可能只与Fe3+反应,也可能与Fe3+反应,剩余部分与Cu2+反应生成铜,所以可能有固体析出,故B错误;
C.若有固体存在,固体中一定有铜,可能有铁,溶液中一定有含有Fe2+,故C正确;
D.当加入的铁较少时,只发生Fe+2Fe3+=3Fe2+时,不会有铜析出,故D错误;
故选C.
B.若溶液中有Cu2+,加入的铁量不足,可能只与Fe3+反应,也可能与Fe3+反应,剩余部分与Cu2+反应生成铜,所以可能有固体析出,故B错误;
C.若有固体存在,固体中一定有铜,可能有铁,溶液中一定有含有Fe2+,故C正确;
D.当加入的铁较少时,只发生Fe+2Fe3+=3Fe2+时,不会有铜析出,故D错误;
故选C.
点评:本题考查氧化还原反应的计算,为高频考点,把握氧化还原反应的先后顺序为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对下列定量实验中的基本操作和仪器的描述正确的是( )
| A、用托盘天平称取 NaOH固体20.0 g |
| B、将用水润湿的pH试纸,浸入稀盐酸溶液,测定溶液的pH |
| C、滴定管的0刻度线在上部,而量筒的0刻度线在下部 |
| D、在配制一定物质的量浓度的溶液时,定容后,经摇匀后发现液面低于刻度线,此时再加入蒸馏水使其液面与刻度持平 |
某二元弱酸的酸式盐NaHA溶液,若pH<7,则溶液中各粒子的浓度关系不正确的是( )
| A、c(Na+)>c(HA-)>c(H+)>c(A2-)>c(H2A) |
| B、c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-) |
| C、c(H+)+c(A2-)=c(OH-)+c(H2A) |
| D、c(Na+)=c(HA-)+c(H2A)+c(A2-) |
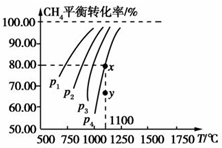 在2L的恒容密闭容器中,充入0.2molCO2和0.2molCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
在2L的恒容密闭容器中,充入0.2molCO2和0.2molCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )| A、上述反应的△H>0 |
| B、压强:P4>P3>P2>P1 |
| C、1100℃,P1时该反应平衡常数约为16.4 |
| D、压强为p4时,在y点:V正>V逆 |

 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是