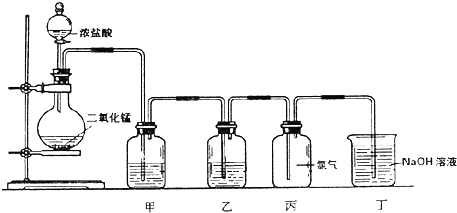
题目内容
9.下列说法正确的是( )| A. | 鉴别溶液中是否有SO42-,先用盐酸酸化,再加BaCl2溶液 | |
| B. | 干馏、分馏都是物理变化 | |
| C. | 往制备乙酸乙酯反应后的混合液中加入Na2CO3溶液,产生气泡,说明乙酸有剩余 | |
| D. | 3 mol Fe在足量的水蒸气中完全反应转移9NA个电子 |
分析 A.先加入盐酸可排除亚硫酸根离子和银离子的干扰;
B.分馏为物理变化;
C.制备乙酸乙酯的反应为可逆反应;
D.铁和水反应生成四氧化三铁.
解答 解:A.先加入盐酸可排除亚硫酸根离子和银离子的干扰,再加入氯化钡可检验是否含有硫酸根离子,故A正确;
B.分馏根据物质的沸点进行分离,为物理变化,故B错误;
C.制备乙酸乙酯的反应为可逆反应,乙酸不能完全反应,故C错误;
D.铁和水反应生成四氧化三铁,3 mol Fe在足量的水蒸气中完全反应转移8NA个电子,故D错误.
故选A.
点评 本题考查较为综合,涉及物质的检验、分离、制备等知识,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握物质的性质,难度不大.

练习册系列答案
相关题目
19.下列实验或操作正确的是( )
| A. | 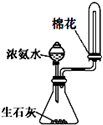 制取氨气 | B. |  蒸发、浓缩、结晶 | C. |  滴定分析 | D. | 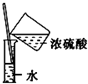 配制稀硫酸 |
20.下列关于除杂说法不正确的是( )
| A. | 除去溴乙烷中的溴,不能用氢氧化钠溶液,应该先加入亚硫酸氢钠溶液洗涤,再分液的方法,反应方程式为:Br2+NaHSO3+H2O═2HBr+NaHSO4 | |
| B. | 除去溴苯中的苯、溴单质,应该先加入氢氧化钠溶液,再分液,最后蒸馏的方法,反应方程式为:Br2+2NaOH=NaBr+NaBrO+H2O | |
| C. | 除去硝基苯中的酸,应该先用水洗去大量的酸,分液后用氢氧化钠溶液除去溶解在有 机层中少量的酸,再用水洗去残留的氢氧化钠和盐,分液后蒸馏,离子方程式为:H++OH-=H2O | |
| D. | 除去苯甲酸中的氯化钠,应先加水溶解,趁热过滤后将滤液迅速降温,加热蒸发溶剂除去氯化钠 |
17.粗盐精制的实验中,没有用到的仪器是( )
| A. | 酒精灯 | B. | 漏斗 | C. | 蒸发皿 | D. | 容量瓶 |
4.将金属钠分别投入下列物质的水溶液中,既有气体又有沉淀生成的是( )
| A. | MgCl2 | B. | K2SO4 | C. | NaCl | D. | HCl |
14.短周期元素X的气态氢化物的化学式为H2X,则X属于( )
| A. | IV A族 | B. | V A族 | C. | VI A族 | D. | VII A族 |
1.在25℃的纯水中,水的离子积(KW)为( )
| A. | KW=1×10-14 | B. | 大于1×10-14 | C. | 小于1×10-14 | D. | 0.01 |
8.用玻璃棒蘸浓硫酸滴在纸上,纸变黑,这表现了浓硫酸的( )
| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 |