题目内容
5.下列解释事实的方程式不正确的是( )| A. | 测0.1 mol/L氨水的pH为11:NH3•H2O?NH4++OH- | |
| B. | 将Na块放入水中,产生气体:2Na+2H2O═2NaOH+H2↑ | |
| C. | 用CuCl2溶液做导电实验,灯泡发光:CuCl2═Cu2++2Cl- | |
| D. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
分析 A.一水合氨为弱电解质,部分电离,应可逆号;
B.钠与水反应生成氢氧化钠和氢气;
C.电解氯化铜反应生成铜和氯气;
D.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气.
解答 解:A.测0.1 mol/L氨水的pH为11,说明一水合氨为弱电解质,部分电离,电离方程式:NH3•H2O?NH4++OH-,故A正确;
B.将Na块放入水中,产生气体,离子方程式:2Na+2H2O═2NaOH+H2↑,故B正确;
C.用CuCl2溶液做导电实验,灯泡发光,电解离子方程式:CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑,故C错误;
D.Al片溶于NaOH溶液中,产生气体,离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑,故D正确;
故选:C.
点评 本题考查了离子方程式书写,涉及电离方程式、电解方程式书写,明确反应实质是解题关键,题目难度不大.

练习册系列答案
相关题目
15.下列说法不正确的是( )
| A. | 目前加碘食盐中含碘元素的物质主要是KIO3 | |
| B. | 维生素C具有还原性,可用作食品抗氧化剂 | |
| C. | 向含有Hg2+的废水中加入Na2S,使Hg2+转化成HgS沉淀除去 | |
| D. | 淀粉、油脂和蛋白质都是天然高分子化合物,都能发生水解反应 |
16.下列物质中,不能由单质直接化合生成的是( )
①CuS ②NH3 ③SO3 ④FeCl3 ⑤NO2.
①CuS ②NH3 ③SO3 ④FeCl3 ⑤NO2.
| A. | ①③⑤ | B. | ①②③⑤ | C. | ①②④⑤ | D. | 全部 |
20.下列物质分类的正确组合是( )
| 选项 | 纯净物 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | 碱石灰 | 烧碱 | 氧化铝 | 二氧化碳 |
| B | NH3•H2O | 小苏打 | 氧化镁 | 二氧化氮 |
| C | 五水硫酸铜 | 纯碱 | 氧化钠 | 三氧化硫 |
| D | H2O2 | 苏打 | 过氧化钠 | 二氧化硫 |
| A. | A | B. | B | C. | C | D. | D |
10.地球表面十公里厚的地层中,含钛元素达千分之六,比铜多61倍,金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系,列反应可以制得Ti3N4和纳米TiO2(如图1).
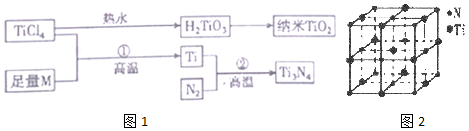
图中的M是短周期金属元素,M的部分电离能如表:
请回答下列问题:
(1)TiO2为离子晶体,己知晶体中阳离子的配位数为6,阴离子的配位数为3,则阳离子的电子排布式为1s22s22p63s23p6
(2)金属Ti与金属M的晶体原子堆积模式相同,其堆积模型为六方最密堆积 (填写堆积模型名称),晶体中原子在二维平面里的配位数为6
(3)室温下TiCl4为无色液体,沸点为136.4℃,由此可知其晶体类型为分子晶体,构成该晶体的粒子的空间构型为正四面体
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如2图所示,已知该氮化钛的密度为p g•cm-3,则该晶胞中N、Ti之间的最近距离为$\frac{1}{2}\root{3}{\frac{4×62}{ρ{N}_{A}}}×1{0}^{10}$ pm,(NA为阿伏加德常数的数值,只列算式).该晶体中与Ti原子距离相等且最近的Ti原子有12 个.
(5)科学家通过X射线探明KC1、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
KC1、CaO、TiN三种离子晶体硬度由低到该的顺序为KCl<CaO<TiN.

图中的M是短周期金属元素,M的部分电离能如表:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/(kJ•mol-1) | 738 | 1451 | 7733 | 10 540 | 13 630 |
(1)TiO2为离子晶体,己知晶体中阳离子的配位数为6,阴离子的配位数为3,则阳离子的电子排布式为1s22s22p63s23p6
(2)金属Ti与金属M的晶体原子堆积模式相同,其堆积模型为六方最密堆积 (填写堆积模型名称),晶体中原子在二维平面里的配位数为6
(3)室温下TiCl4为无色液体,沸点为136.4℃,由此可知其晶体类型为分子晶体,构成该晶体的粒子的空间构型为正四面体
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如2图所示,已知该氮化钛的密度为p g•cm-3,则该晶胞中N、Ti之间的最近距离为$\frac{1}{2}\root{3}{\frac{4×62}{ρ{N}_{A}}}×1{0}^{10}$ pm,(NA为阿伏加德常数的数值,只列算式).该晶体中与Ti原子距离相等且最近的Ti原子有12 个.
(5)科学家通过X射线探明KC1、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
| 离子晶体 | NaCl | KC1 | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
17.设NA表示阿伏加德罗常数的值.下列有关说法中正确的是( )
| A. | 常温常压下,46 gN2O4中含氧原子数为2NA | |
| B. | 常温常压下,11.2 LNH3中含共价键的数目为1.5NA | |
| C. | 电解精炼铜阳极质量减少32 g时电路中转移电子总数为NA | |
| D. | 1 L 0.2 mol/LNa2SO4溶液中含有阴阳离子总数为0.6NA |
1.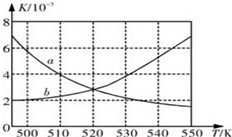 Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g)△H=-198kJ/mol.
(1)如图所示能正确反应平衡常数K随温度变化关系的曲线是a(填曲线标记字母),其判断理由是正反应放热,温度升高,平衡常数减小.
(2)在一定温度下,向2.0L固定的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g) 达到平衡.反应过程中测得的部分数据见下表:
①0-20min的平均反应速率V(co)=7.5×10-3mol/(L•min);
②达平衡时,H2 的转化率为:80%;
③在上述温度下,向平衡后的2L容器中再充入0.4molH2 和0.4molCH3OCH3 (g),则化学平衡正向(向“正向”、“逆向”或“不”)移动.
(3)用Li2CO3 和Na2CO3 的熔融盐混合物作为电解质,CO为负极燃气,空气与CO2 的混合气体作为正极助燃气,制得在650℃工作的燃料电池,则负极反应式为:2CO+2CO32--4e-=4CO2当燃料电池的电路中有0.2NA个电子发生转移,则标况下生成2.24升CO2.
Ⅱ:已知在25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20,在25℃下,向浓度均为0.1mol/L的MgCl2 和CuCl2 混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀(填化学式)生成该沉淀的离子方程式为Cu2++2NH3•H2O?Cu(OH)2↓+2NH4+.
 Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)CH3OCH3(g)+H2O(g)△H=-198kJ/mol.
(1)如图所示能正确反应平衡常数K随温度变化关系的曲线是a(填曲线标记字母),其判断理由是正反应放热,温度升高,平衡常数减小.
(2)在一定温度下,向2.0L固定的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g) 达到平衡.反应过程中测得的部分数据见下表:
| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | - |
| n(CO)/mol | 1.0 | - | 0.425 | 0.2 | 0.2 |
| n(CH3OCH3)/mol | 0 | 0.15 | - | - | 0.4 |
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
②达平衡时,H2 的转化率为:80%;
③在上述温度下,向平衡后的2L容器中再充入0.4molH2 和0.4molCH3OCH3 (g),则化学平衡正向(向“正向”、“逆向”或“不”)移动.
(3)用Li2CO3 和Na2CO3 的熔融盐混合物作为电解质,CO为负极燃气,空气与CO2 的混合气体作为正极助燃气,制得在650℃工作的燃料电池,则负极反应式为:2CO+2CO32--4e-=4CO2当燃料电池的电路中有0.2NA个电子发生转移,则标况下生成2.24升CO2.
Ⅱ:已知在25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20,在25℃下,向浓度均为0.1mol/L的MgCl2 和CuCl2 混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀(填化学式)生成该沉淀的离子方程式为Cu2++2NH3•H2O?Cu(OH)2↓+2NH4+.
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 11.2 L CO2所含分子数为0.5 NA | |
| B. | 32gO2和O3的混合气体中含有的氧原子数为2NA | |
| C. | 标况下,11.2L乙醇(C2H5OH)中所含的碳原子数目为NA | |
| D. | 14.2 g Na2SO4固体中阴离子所带电荷数为0.1NA |