题目内容
灰锡(以粉末状存在)和白锡是锡的两种同素异形体.已知:
①Sn(s、白)+2HCl(aq)═SnCl2(aq)+H2(g)△H1
②Sn(s、灰)+2HCl(aq)═SnCl2(aq)+H2(g)△H2
③Sn(s、灰) Sn(s、白)△H3=+2.1kJ/mol,下列说法正确的是( )
Sn(s、白)△H3=+2.1kJ/mol,下列说法正确的是( )
①Sn(s、白)+2HCl(aq)═SnCl2(aq)+H2(g)△H1
②Sn(s、灰)+2HCl(aq)═SnCl2(aq)+H2(g)△H2
③Sn(s、灰)
 Sn(s、白)△H3=+2.1kJ/mol,下列说法正确的是( )
Sn(s、白)△H3=+2.1kJ/mol,下列说法正确的是( )| A、△H1>△H2 |
| B、锡制器皿长期处于低于13.2℃的环境中,会自行毁坏 |
| C、锡在常温下以灰锡状态存在 |
| D、灰锡转化为白锡的反应是放热反应 |
考点:反应热和焓变,反应热的大小比较
专题:
分析:A、利用盖斯定律来判断反应的焓变大小;
B、根据反应③当温度低于13.2℃的环境时Sn的转化来判断;
C、根据反应的焓变来确定反应是吸热还是放热;
D、根据③来判断反应的焓变大小.
B、根据反应③当温度低于13.2℃的环境时Sn的转化来判断;
C、根据反应的焓变来确定反应是吸热还是放热;
D、根据③来判断反应的焓变大小.
解答:
解:A、根据③:Sn(s、灰) Sn(s、白)△H3=+2.1kJ?mol-1,则②-①=③,所以△H2-△H1=△H3>0,所以△H1<△H2,故A错误;
Sn(s、白)△H3=+2.1kJ?mol-1,则②-①=③,所以△H2-△H1=△H3>0,所以△H1<△H2,故A错误;
B、根据③:Sn(s、灰) Sn(s、白)△H3=+2.1kJ?mol-1,当温度低于13.2℃的环境时,白锡会转化为灰锡,灰锡为粉末状,所以会自行毁坏,故B正确;
Sn(s、白)△H3=+2.1kJ?mol-1,当温度低于13.2℃的环境时,白锡会转化为灰锡,灰锡为粉末状,所以会自行毁坏,故B正确;
C、根据③:Sn(s,灰) Sn(s,白)△H3=+2.1kJ?mol-1,则锡在常温下以白锡状态存在,故C错误;
Sn(s,白)△H3=+2.1kJ?mol-1,则锡在常温下以白锡状态存在,故C错误;
D、根据③:Sn(s,灰) Sn(s,白)△H3=+2.1kJ?mol-1,焓变大于0,所以灰锡转为白锡的反应是吸热反应,故D错误.
Sn(s,白)△H3=+2.1kJ?mol-1,焓变大于0,所以灰锡转为白锡的反应是吸热反应,故D错误.
故选B.
 Sn(s、白)△H3=+2.1kJ?mol-1,则②-①=③,所以△H2-△H1=△H3>0,所以△H1<△H2,故A错误;
Sn(s、白)△H3=+2.1kJ?mol-1,则②-①=③,所以△H2-△H1=△H3>0,所以△H1<△H2,故A错误;B、根据③:Sn(s、灰)
 Sn(s、白)△H3=+2.1kJ?mol-1,当温度低于13.2℃的环境时,白锡会转化为灰锡,灰锡为粉末状,所以会自行毁坏,故B正确;
Sn(s、白)△H3=+2.1kJ?mol-1,当温度低于13.2℃的环境时,白锡会转化为灰锡,灰锡为粉末状,所以会自行毁坏,故B正确;C、根据③:Sn(s,灰)
 Sn(s,白)△H3=+2.1kJ?mol-1,则锡在常温下以白锡状态存在,故C错误;
Sn(s,白)△H3=+2.1kJ?mol-1,则锡在常温下以白锡状态存在,故C错误;D、根据③:Sn(s,灰)
 Sn(s,白)△H3=+2.1kJ?mol-1,焓变大于0,所以灰锡转为白锡的反应是吸热反应,故D错误.
Sn(s,白)△H3=+2.1kJ?mol-1,焓变大于0,所以灰锡转为白锡的反应是吸热反应,故D错误.故选B.
点评:本题考查学生盖斯定律的应用以及物质的能量和其稳定性之间的关系,侧重于基础知识的考查,难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、4℃时,5.4mL水中所含的水分子数是0.3NA(4℃时,水的密度为1.0g/ml) |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为 NA |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3 NA |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍.下列说法正确的是( )
| A、X的氢化物溶于水显酸性 |
| B、X与Y形成化合物的化学式为X2Y3 |
| C、Y的氧化物是离子化合物 |
| D、X和Z的最高价氧化物对应的水化物都是弱酸 |
下列指定反应的离子方程式正确的是( )
| A、铜溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B、氯气和水的反应:Cl2+H2O=2H++Cl-+ClO- |
| C、用氨水溶解氯化银沉淀:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O |
| D、将过量二氧化硫通入氨水中:SO2+NH3?H2O=HSO3-+NH4+ |
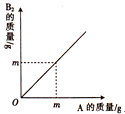 已知反应aA+B2=aAB,M(A)、M(B2)、M(AB)分别表示A、B2和AB的摩尔质量,其单位均为g/mol.A与B2反应的质量关系如图所示.下列说法中正确的是( )
已知反应aA+B2=aAB,M(A)、M(B2)、M(AB)分别表示A、B2和AB的摩尔质量,其单位均为g/mol.A与B2反应的质量关系如图所示.下列说法中正确的是( )| A、无法确定计量数a的大小 |
| B、M(A)=2M(B2) |
| C、M(AB)=2M(A)+M(B2) |
| D、若有6g A完全反应,则生成AB的质量为12g |
常温下,某溶液中由水电离出的出c(H+)=1.0×10-13mol/L则在该溶液中一定不可以大量共存的一组离子是( )
| A、NH4+、NO3-、K+、SO42- |
| B、CO32_、NO3-、HCO3-、Na+ |
| C、Na+、ClO-、AlO2-、NO3- |
| D、MnO4-、K+、Na+、SO42- |

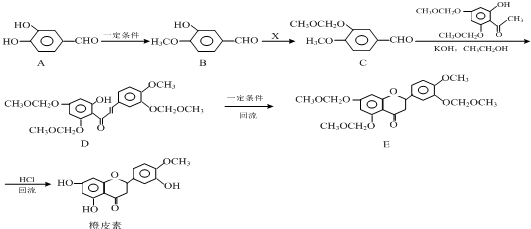
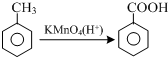 结合流程信息,写出以对甲基苯酚和上述流程中的“X”为原料,制备
结合流程信息,写出以对甲基苯酚和上述流程中的“X”为原料,制备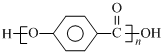 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: