题目内容
10. 常温下有浓度为0.1mol/L,体积为VL的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应.根据图象回答下列问题:
常温下有浓度为0.1mol/L,体积为VL的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应.根据图象回答下列问题:(1)上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH如下表,请将表格补充完整:
| 离子浓度大小顺序 | 溶质化学式 | 溶液的pH |
| c (NH4+)>c (OH-)>c (CI-)>c (H+) | ① | >7 |
| ② | ③ | =7 |
| ④ | NH4Cl | ⑤ |
(3)若取该实验中恰好完全反应的d点溶液,向其中滴加0.1VL某浓度的氨水后溶液呈中性,依(2)中计算结果计算所滴加氨水的浓度为0.01 moI/L.
分析 (1)由图象可知,点b反应后溶液是NH4C1与NH3•H2O物质的量之比为1:1的混合物,溶液呈碱性,说明NH3•H2O电离程度大于NH4C1的水解程度,由电荷守恒可知:c(C1-)+c(OH-)=c(NH4+)+c(H+),物料守恒为:2c(Cl-)=c(NH4+)+c(NH3.H2O),质子守恒为:2c(OH-)+c(NH3.H2O)=c(NH4+)+2c(H+);由电荷守恒可知:c(C1-)+c(OH-)=c(NH4+)+c(H+),由图象可知,点c pH=7,点d体积相同,则恰好完全反应生成NH4Cl,利用盐的水解来分析溶液呈酸性,则c(Cl-)>c(NH4+)>c(H+)>c(OH-);当NH3•H2O较多,滴入的 HCl较少时,生成NH4C1少量,溶液中NH3•H2O浓度远大于NH4C1浓度,可能出现;在d点,氨水和盐酸恰好完全反应,得到氯化铵溶液,显示酸性,据此回答.
(2)根据滴定前氨水中c(H+)=10-11mol/L,利用水的离子积得c(OH-)然后根据氨水的电离平衡常数的表达式进行计算;
(3)加入氨水后溶液呈中性,根据物料守恒得到答案.
解答 解:(1)由图象可知,点b反应后溶液是NH4C1与NH3•H2O物质的量之比为1:1的混合物,溶液呈碱性,说明NH3•H2O电离程度大于NH4C1的水解程度,由电荷守恒可知:c(C1-)+c(OH-)=c(NH4+)+c(H+),物料守恒为:2c(Cl-)=c(NH4+)+c(NH3.H2O),质子守恒为:2c(OH-)+c(NH3.H2O)=c(NH4+)+2c(H+);由电荷守恒可知:c(C1-)+c(OH-)=c(NH4+)+c(H+),由图象可知,点c pH=7,点d体积相同,则恰好完全反应生成NH4Cl,利用盐的水解来分析溶液呈酸性,则c(Cl-)>c(NH4+)>c(H+)>c(OH-);当NH3•H2O较多,滴入的 HCl较少时,生成NH4C1少量,溶液中NH3•H2O浓度远大于NH4C1浓度,可能出现,在d点,氨水和盐酸恰好完全反应,得到氯化铵溶液,显示酸性,故答案为:
| 离子浓度大小顺序 | 溶质化学式 | 溶液的pH |
| NH3•H2O、NH4Cl | ||
| c(NH4+)=c(Cl-)>c(OH-)=c(H+) | NH3•H2O、NH4Cl | |
| c(Cl-)>c(NH4+)>c(H+)>c(OH-) | <7 |
故答案为:10-5;1;
(3)向其中滴加AL某浓度的氨水后溶液呈中性,则溶液中c(Cl-)=c(NH4+)=$\frac{0.1V}{0.1V+2V}$mol/L,令加入氨水的浓度为amol/L,根据氮元素守恒可知,溶液中c(NH3.H2O)=($\frac{0.1V+0.1a}{2.1V}$-$\frac{0.1V}{0.1V+2V}$)mol/L,由一水合氨的电离平衡常数可得:c(NH4+)•c(OH-)=Kb•c(NH3.H2O),所以 $\frac{0.1V}{1.2V}$×10-7=10-5×($\frac{0.1V+0.1a}{2.1V}$-$\frac{0.1V}{0.1V+2V}$),解得a=0.01mol/L,
故答案为:0.01.
点评 本题考查了弱电解质的电离,涉及弱电解质溶液的稀释、酸碱混合溶液定性判断、电离平衡常数的计算等知识点,根据弱电解质的电离特点、溶液酸碱性结合元素守恒来分析解答,难点是(3)题,根据电荷守恒、元素守恒结合电离平衡常数解答,题目难度中等.

| A. | NaCl | B. | CO2 | C. | H2SO4 | D. | H2O |
| A. | 氢氧化钠溶液 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 氯化钠溶液 |
①Al2(SO4)3和KOH ②稀盐酸和稀Na2CO3
③NaAlO2和H2SO4 ④Ba(OH)2和NaHCO3.
| A. | ① | B. | ①③ | C. | ①②③ | D. | ①②③④ |
| A. | n(CH3COOH) | B. | c(H+) | C. | c(H+)•c(OH-) | D. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ |
| A. | 10 | B. | 11 | C. | 12 | D. | 13 |
| A. | 常温常压下,78gNa2O2中含有的阴离子数是NA | |
| B. | m g ${\;}_{Z}^{A}$Xn-中所含电子数为(Z-n)mNA/A | |
| C. | 1L0.1mol/LFe(OH)3胶体中含有Fe(OH)3胶粒数为0.1NA | |
| D. | H2SO4的摩尔质量为98 |
| A. | 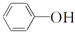 与 与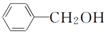 是同系物 是同系物 | |
| B. | 乙酸乙酯(CH3COOCH2CH3)的核磁共振氢谱出现三组峰,且峰面积之比为3:2:3 | |
| C. | 分子式为C4H10的有机物一氯代物共有8种 | |
| D. | 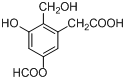 含氧官能团有4种 含氧官能团有4种 |
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-6mol•L-1 | |
| B. | pH相等的①NH4C1、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③ | |
| C. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL |