题目内容
现有一含少量铁、硅的铝合金,取等质量的两份样品,分别投入足量的盐酸和稀氢氧化钠溶液中,放出等量的氢气,则该合金中铁与硅的关系正确的是(已知:Si+2NaOH+H2O====Na2SiO3+2H2↑) ( )
①物质的量之比为2∶1 ②物质的量之比为3∶1
③质量之比为2∶1 ④质量之比为4∶1
A.②④ B.②③ C.①④ D.只有④
C
【解析】
试题分析:将等质量的合金分别投入足量盐酸和稀氢氧化钠溶液中时,铝与盐酸和氢氧化钠反应生成的氢气相等,铁仅与盐酸反应生成氢气,反应方程式是Fe+2HCl FeCl2+H2↑,硅仅与氢氧化钠反应生成氢气,反应方程式是Si+2NaOH+H2O
FeCl2+H2↑,硅仅与氢氧化钠反应生成氢气,反应方程式是Si+2NaOH+H2O Na2SiO3+2H2↑。由于放出等量的氢气,因此铁与硅的物质的量之比应为2∶1,质量之比为4∶1,故选C。
Na2SiO3+2H2↑。由于放出等量的氢气,因此铁与硅的物质的量之比应为2∶1,质量之比为4∶1,故选C。
考点:铝及铝合金

练习册系列答案
相关题目
 +
+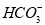 +2OH-====NH3·H2O+
+2OH-====NH3·H2O+ +H2O
+H2O