题目内容
5.用蒸馏水稀释0.1mol•L-1的醋酸至0.01mol•L-1,稀释过程中温度维持25℃不变,下列各项中始终保持增大趋势的是( )| A. | c(H+)•c(OH-) | B. | c(OH-) | ||
| C. | $\frac{c({H}^{+}•c(C{H}_{3}CO{O}^{-}))}{c(C{H}_{3}COOH)}$ | D. | $\frac{c(C{H}^{+})}{c(C{H}_{3}COOH)}$ |
分析 醋酸溶液中存在CH3COOH?CH3COO-+H+,加水稀释促进电离,n(CH3COO-)和n(H+)增大,n(CH3COOH)减小,结合溶液体积变化以及物质的量之比等于浓度之比解答该题.
解答 解:醋酸溶液中存在CH3COOH?CH3COO-+H+,加水稀释促进电离,
A.由Kw=c(H+)×c(OH-)可知,温度不变,则c(H+)c(OH-)不变,故A错误;
B.加水稀释,醋酸酸性减弱,c(OH-)增大,故B正确;
C.$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$为醋酸的电离常数,温度不变,常数不变,故C错误;
D.加水稀释促进电离,n(CH3COO-)和n(H+)增大,n(CH3COOH)减小,则$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$=$\frac{n({H}^{+})}{n(C{H}_{3}COOH)}$,应增大,故D正确;
故选BD.
点评 本题考查弱电解质的电离,侧重于学生的分析能力的考查,为高考常见题型,注意把握弱电解质的电离特点以及影响因素,难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
14.下列说法正确的是( )
| A. | 升高温度,正反应速率增大,逆反应速率减小 | |
| B. | 在温度和体积一定的情况下,通入氦气化学反应速率不变 | |
| C. | 增大压强可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| D. | 使用催化剂,可以改变反应的△H |
15.下列各组物质互为同素异形体的是( )
| A. | 12C和14C | B. | H2O和D2O | C. | O2和O3 | D. | 淀粉和纤维素 |
20.晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等,.以下是工业上制取纯硅的一种方法.

已知:在一定条件下可发生反应:Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H<0
Ⅰ.反应②、③均需要加热,有如下两个温度区间分别供两反应选择,你认为反应②应选择a
(填序号字母),原因是因反应Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H<0,温度较低时反应向正向进行程度较大,有利于SiHCl3的生成;
a.520~530K b.1350~1360K
Ⅱ.现在实验室模拟工业上粗硅提纯的过程,已知SiHCl3遇水强烈水解,其他相关数据如下表所示:
(1)现用如下装置(如图1)进行模拟反应②的过程.实验室制HCl的反应原理为:
2NaCl(s)+H2SO4(浓) QUOTE 2HCl↑+Na2SO4
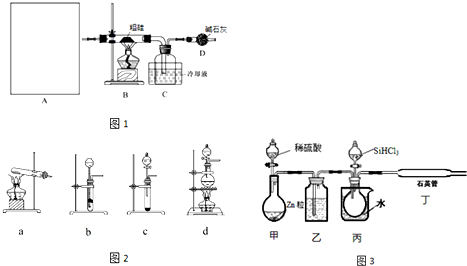
A中是HCl的发生装置,你认为应选择下列哪套装置?d(填装置的序号字母),装置D中碱石灰的作用为吸收剩余HCl、防止空气中的水蒸气进入C装置造成SiHCl3的水解;
(2)已知液态粗品SiHCl3中含有杂质SiCl4、AlCl3、FeCl3等,则流程中操作①为分馏(填操作名称),下列不是该操作所需的仪器是(如图2)bd(填装置序号字母);
a.冷凝管 b.圆底烧瓶 c.蒸馏烧瓶 d.分液漏斗 e.温度计 f.接受器
(3)用SiHCl3与H2反应制备纯硅的装置如图3:
①按图示组装好仪器后,下列实验步骤的正确顺序为dbacef(填步骤的序号字母),
a.打开甲装置分液漏斗旋塞,滴加稀硫酸,反应生成H2;
b.向装置中添加药品;
c.打开丙装置分液漏斗的旋塞,滴加SiHCl3,并加热相应装置;
d.检查装置气密性;
e.停止向丙装置滴加SiHCl3,并停止加热相应装置;
f.停止通H2;
步骤c中需要加热的装置为丙、丁(填装置序号“甲”、“乙”、“丙”、“丁”)
②该套装置的设计缺陷是无尾气处理装置.

已知:在一定条件下可发生反应:Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H<0
Ⅰ.反应②、③均需要加热,有如下两个温度区间分别供两反应选择,你认为反应②应选择a
(填序号字母),原因是因反应Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H<0,温度较低时反应向正向进行程度较大,有利于SiHCl3的生成;
a.520~530K b.1350~1360K
Ⅱ.现在实验室模拟工业上粗硅提纯的过程,已知SiHCl3遇水强烈水解,其他相关数据如下表所示:
| 物质 | SiCl4 | SiHCl3 | AlCl3 | FeCl3 |
| 沸点/℃ | 57.7 | 33.0 | - | 315 |
| 升华温度/℃ | - | - | 180 | 300 |
2NaCl(s)+H2SO4(浓) QUOTE 2HCl↑+Na2SO4

A中是HCl的发生装置,你认为应选择下列哪套装置?d(填装置的序号字母),装置D中碱石灰的作用为吸收剩余HCl、防止空气中的水蒸气进入C装置造成SiHCl3的水解;
(2)已知液态粗品SiHCl3中含有杂质SiCl4、AlCl3、FeCl3等,则流程中操作①为分馏(填操作名称),下列不是该操作所需的仪器是(如图2)bd(填装置序号字母);
a.冷凝管 b.圆底烧瓶 c.蒸馏烧瓶 d.分液漏斗 e.温度计 f.接受器
(3)用SiHCl3与H2反应制备纯硅的装置如图3:
①按图示组装好仪器后,下列实验步骤的正确顺序为dbacef(填步骤的序号字母),
a.打开甲装置分液漏斗旋塞,滴加稀硫酸,反应生成H2;
b.向装置中添加药品;
c.打开丙装置分液漏斗的旋塞,滴加SiHCl3,并加热相应装置;
d.检查装置气密性;
e.停止向丙装置滴加SiHCl3,并停止加热相应装置;
f.停止通H2;
步骤c中需要加热的装置为丙、丁(填装置序号“甲”、“乙”、“丙”、“丁”)
②该套装置的设计缺陷是无尾气处理装置.
15.下列事实与NH3极易溶于水无关的是( )
| A. | NH3与水反应生成NH3•H2O | B. | NH3与水分子之间形成氢键 | ||
| C. | NH3和水分子的相对分子质量接近 | D. | NH3是极性分子 |

 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ/mol.
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ/mol.