题目内容
短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y 的次外层电子数是最外层的 ,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是( )。
,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是( )。
A.原子半径:rW>rZ>rY
B.Y形成的离子与W形成的离子的电子数不可能相同
C.化合物X2Y、ZY、WY3 中化学键的类型相同
D.由X、Y、Z、W组成的化合物的水溶液可能显酸性
D
【解析】
试题分析:X的原子在元素周期表中原子半径最小,所以X是H元素,Y 的次外层电子数是最外层的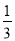 ,所以次外层电子数不可能是8,所以Y的次外层电子数是2也是第一层电子数,则Y是O元素,所以X是H元素,W与Y同主族,所以W是S元素,ZX2是一种储氢材料,可知Z的化合价是+2价,Z是Mg元素。A、根据原子半径的比较,Mg的原子半径最大,其次是S,最小的是O,错误;B、O形成的O22-与S2-的电子数相同,都是18个电子,错误;C、化合物ZY是MgO,属于离子化合物,含有离子键,而其他两种是共价化合物,含有共价键,错误;D、由X、Y、Z、W组成的化合物的水溶液可能显酸性,如Mg(HSO4)2,正确,答案选D。
,所以次外层电子数不可能是8,所以Y的次外层电子数是2也是第一层电子数,则Y是O元素,所以X是H元素,W与Y同主族,所以W是S元素,ZX2是一种储氢材料,可知Z的化合价是+2价,Z是Mg元素。A、根据原子半径的比较,Mg的原子半径最大,其次是S,最小的是O,错误;B、O形成的O22-与S2-的电子数相同,都是18个电子,错误;C、化合物ZY是MgO,属于离子化合物,含有离子键,而其他两种是共价化合物,含有共价键,错误;D、由X、Y、Z、W组成的化合物的水溶液可能显酸性,如Mg(HSO4)2,正确,答案选D。
考点:考查元素的推断及元素、化合物的性质

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目

 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是 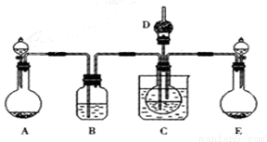


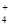 )=c(Cl-)
)=c(Cl-)