题目内容
16.铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4•7H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如图: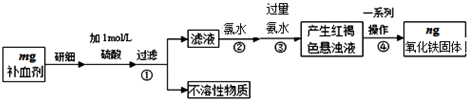
(1)实验中用已经准确量取的浓硫酸配制500mL 1mol•L-1的硫酸溶液,则配制时用到的仪器除烧杯、玻璃棒外,还有两种仪器是500mL容量瓶,胶头滴管.
(2)步骤②加入过量氯水的作用是将Fe2+全部氧化为Fe3+,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-.
(3)步骤④中一系列操作步骤为过滤、洗涤、灼烧、冷却、称量.
(4)若实验无损耗,则该补血剂含铁元素的质量分数为$\frac{70n}{m}$%.
(5)下列操作会导致所测定的铁元素含量偏高的是BC
A.步骤③所加氨水量不足
B.步骤④洗涤不充分
C.步骤④灼烧不充分.
(6)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1mol•L-1的硫酸溶液,过滤.取滤液加KSN溶液,若溶液变成红色,说明该补血剂已变质.
分析 由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量.
(1)用量筒量取浓硫酸体积,在烧杯中稀释,并用玻璃棒搅拌,冷却后引入500mL容量瓶中,洗涤、加水定容,距离刻度线1-2cm改用胶头滴管;
(2)加入过量的氯水将Fe2+完全氧化为Fe3+;
(3)步骤④中一系列处理是由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量;
(4)由Fe元素守恒,根据氧化铁的质量计算铁元素的质量分数;
(5)A.步骤③所加氨水量不足,铁离子不能完全转化为氢氧化铁沉淀;
B.步骤④洗涤不充分,氢氧化铁会附着杂质;
C.步骤④灼烧不充分,氢氧化铁分解不完全,测定氧化铁的质量偏大.
(6)补血剂本质时Fe2+被氧化为Fe3+,Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在.
解答 解:由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量.
(1)用量筒量取浓硫酸体积,在烧杯中稀释,并用玻璃棒搅拌,冷却后引入500mL容量瓶中,洗涤、加水定容,距离刻度线1-2cm改用胶头滴管,配制时用到的仪器除烧杯、玻璃棒外,还有两种仪器是:500mL容量瓶、胶头滴管,
故答案为:500mL容量瓶、胶头滴管;
(2)加入过量的氯水将Fe2+完全氧化为Fe3+,反应离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,
故答案为:将Fe2+全部氧化为Fe3+;2Fe2++Cl2=2Fe3++2Cl-;
(3)步骤④中一系列处理是由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量,
故答案为:洗涤;
(4)最后氧化铁为ag,氧化铁含有铁元素的质量为$\frac{112}{160}$×n g=0.7n g,故补血剂含铁元素的质量分数为$\frac{0.7ng}{mg}$×100%=$\frac{70n}{m}$%,
故答案为:$\frac{70n}{m}$%;
(5)A.步骤③所加氨水量不足,铁离子不能完全转化为氢氧化铁沉淀,测定氧化铁的质量偏小,故铁元素质量分数偏小,故A不符合;
B.步骤④洗涤不充分,氢氧化铁会附着杂质,测定氧化铁的质量偏大,故铁元素质量分数偏高,故B符合;
C.步骤④灼烧不充分,氢氧化铁分解不完全,测定氧化铁的质量偏大,故铁元素质量分数偏高,故C符合,
故选:BC;
(6)补血剂本质时Fe2+被氧化为Fe3+,过滤后取滤液加KSCN溶液,若溶液变成红色,说明该补血剂已变质.
故答案为:KSCN;红.
点评 本题考查物质含量探究实验,设计对实验原理与实验操作的理解、物质分离提纯、元素化合物性质、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子的电子式是
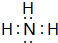 ,其最高价氧化物对应的水化物与其氢化物反应的离子方程式:NH3+H+=NH4+.
,其最高价氧化物对应的水化物与其氢化物反应的离子方程式:NH3+H+=NH4+. (2)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为离子键、共价键.
(3)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法及现象是:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生),证明存在该阳离子.
| A. | 滴定终点读数时俯视读数 | |
| B. | 锥形瓶洗净后未干燥 | |
| C. | 碱式滴定管滴定前尖嘴部分有气泡,滴定后气泡消失 | |
| D. | 酸式滴定管使用前,水洗后未用待测盐酸润洗 |
| A. | CH3CH2CH2CH2CH3 | B. | 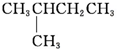 | C. |  | D. | 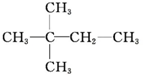 |
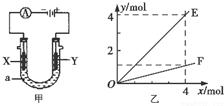
| A. | 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 | |
| B. | 按图甲装置用惰性电极电解AgN03溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 | |
| C. | 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol | |
| D. | 若X、Y为铂电极.a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol•L-1 |
 苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸.反应方程式如下:
苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸.反应方程式如下: +2KMnO4 $\stackrel{△}{→}$
+2KMnO4 $\stackrel{△}{→}$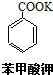 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O 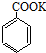 +HCl→
+HCl→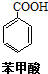 +KCl
+KCl已知有关化合物的相关数据如表所示:
| 化合物 | 相对分子质量 | 密度(g•cm-3) | 溶解性 | 沸点(℃) |
| 甲苯 | 92 | 0.87 | 难溶于水 | 110.0 |
| 苯甲酸钾 | 160 | - | 易溶于水 | - |
| 苯甲酸 | 122 | 1.26 | 微溶于水 | 248.0 |
合成:如图(固定及加热装置略去)所示,在三颈烧瓶中加入4.23mL甲苯和100mL蒸馏水,瓶口装上温度计、电动搅拌器、冷凝管,慢慢开启电动搅拌器,加热至沸腾.经冷凝管上口分批加入21.30g高锰酸钾(过量),继续煮沸至甲苯层消失,回流液中不再出现油珠为止,得到反应混合物.
对反应混合物进行分离:①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤.
对粗产品苯甲酸进行提纯:①沸水溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥.
请回答下列有关问题:
(1)实验中准确量取4.23mL甲苯所需仪器为酸式滴定管.
(2)冷凝管的上口是否需要塞上塞子否(填“是”或“否”),a处水流方向是进水(填“进水”或“出水”).
(3)高锰酸钾需要分批加入,请用化学反应速率观点说明理由避免反应过快,使反应液从回流管上端喷.
(4)在对粗产品苯甲酸进行提纯过程中,“③趁热过滤”的目的是除去活性炭,减少苯甲酸结晶析出;“④”的操作名称是冷却结晶;可证明“⑥洗涤”步骤已洗涤干净的方法是取最后一次洗涤液,加入用HNO3酸化的AgNO3溶液,若无白色沉淀生成,说明沉淀已洗涤干净.
(5)干燥后称量得苯甲酸2.93g,则苯甲酸的产率为60%.