题目内容
在标准状况下,将224L HCl气体溶于635mL水中,所得盐酸的密度为1.18g?cm-3.试计算:
①所得盐酸物质的量浓度是 .
②取出这种盐酸10mL,稀释至118L,所得稀盐酸的物质的量浓度是 .如取10mL盐酸时仰视其他操作均正确得稀盐酸浓度 .(填“偏大”、“等于”、“偏小”)
③在40.0mL 0.065mol?L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡.若使反应不产生CO2气体,加入稀盐酸的体积最多不超过 mL.
①所得盐酸物质的量浓度是
②取出这种盐酸10mL,稀释至118L,所得稀盐酸的物质的量浓度是
③在40.0mL 0.065mol?L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡.若使反应不产生CO2气体,加入稀盐酸的体积最多不超过
考点:物质的量浓度的相关计算
专题:计算题
分析:①(1)根据n=
计算HCl的物质的量,根据m=nM计算HCl的质量,根据m=ρV计算水的质量,进而计算溶液的体积,结合V=
计算溶液的体积,再根据c=
计算盐酸物质的量浓度;
②根据稀释定律C浓V浓=C稀V稀来计算;根据C=
并结合n的变化来分析;
③根据反应Na2CO3+HCl═NaHCO3+NaCl计算.
| V |
| Vm |
| m |
| ρ |
| n |
| V |
②根据稀释定律C浓V浓=C稀V稀来计算;根据C=
| n |
| V |
③根据反应Na2CO3+HCl═NaHCO3+NaCl计算.
解答:
解:①(1)n(HCl)=
=10mol,m(HCl)=10mol×36.5g/mol=365g,
溶液质量为365g+635mL×1g/mL=1000g,
则溶液的体积为
=0.847L,
则c(HCl)=
=11.8mol/L,
故答案为:11.8mol/L;
②设稀释后稀盐酸的物质的量浓度为xmol/L,根据稀释定律C浓V浓=C稀V稀可知:
11.8mol/L×0.01L=Xmol/L×118L
解得:X=0.001mol/L;
如取10mL盐酸时仰视,会导致所取的浓盐酸的体积偏大,故所配的稀盐酸浓度偏大.
故答案为:0.001mol/L;偏大;
③n(Na2CO3)=0.040L×0.065mol?L-1=0.0026 mol,
设加入稀盐酸的体积最多不超过x mL,则n(HCl)=1mol?L-1×0.001x L=0.001x mol,
根据反应Na2CO3+HCl═NaHCO3+NaCl,可得0.0026=0.001x,解得x=2.6,
故答案为:2.6.
| 224L |
| 22.4L/mol |
溶液质量为365g+635mL×1g/mL=1000g,
则溶液的体积为
| 1000g |
| 1180g/L |
则c(HCl)=
| 10mol |
| 0.847L |
故答案为:11.8mol/L;
②设稀释后稀盐酸的物质的量浓度为xmol/L,根据稀释定律C浓V浓=C稀V稀可知:
11.8mol/L×0.01L=Xmol/L×118L
解得:X=0.001mol/L;
如取10mL盐酸时仰视,会导致所取的浓盐酸的体积偏大,故所配的稀盐酸浓度偏大.
故答案为:0.001mol/L;偏大;
③n(Na2CO3)=0.040L×0.065mol?L-1=0.0026 mol,
设加入稀盐酸的体积最多不超过x mL,则n(HCl)=1mol?L-1×0.001x L=0.001x mol,
根据反应Na2CO3+HCl═NaHCO3+NaCl,可得0.0026=0.001x,解得x=2.6,
故答案为:2.6.
点评:本题考查物质的量浓度计算、化学方程式的有关计算,注意公式的运用,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定条件下,在容积固定的某密闭容器中发生的反应N2+3H2?2NH3.在10s内N2的浓度由5mol/L降至4mol/L.下列说法正确的是 ( )
| A、用NH3表示的化学反应速率为0.1 mol/(L?s) |
| B、维持容积的体积不变充入氩气,会加快该反应的速率 |
| C、增加H2的浓度该正反应速率和逆反应速率都会加快 |
| D、反应足够长时间,N2、H2中至少有一种物质浓度降为零 |

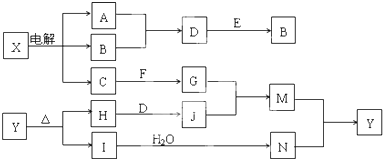
 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位. :
: :
: :
: :
: