题目内容
2.甲醛分子(CH2O)的中心原子(碳原子)的价层电子对数为3,其孤电子对数为0,则该分子呈平面三角形形.甲醛分子的中心原子的杂化类型为sp2杂化,分子中共有3个σ键,有1个π键,其中C-H的σ键的类型为sp2-s,C-O的σ键的类型为sp2-p.分析 根据杂化轨道理论分析,杂化轨道用于成σ键和填充孤电子对,甲醛分子中心原子为C原子,价层电子对数等于σ键+孤电子对,价层电子对数为2+1=3,sp2杂化,不含孤电子对,为平面三角形,单键为σ键,双键有一个σ键和1个π键.
解答 解:HCHO中C原子成2个C-H键、1个C=O双键,单键为σ键,双键有一个σ键和1个π键,故含有3个σ键和1个π键杂,价层电子对数为2+1=3,不含孤电子对,杂化轨道数为3,C原子采取sp2杂化,为平面三角形,其中C-H的σ键是C的sp2轨道与H的s轨道形成,类型为sp2-s,C-O的σ键为C的sp2轨道与O的p轨道性,类型为sp2-p,
故答案为:3;0;平面三角形; sp2杂化;3;1;sp2-s;sp2-p.
点评 本题考查杂化轨道、价层电子对互斥理论、共价键中的σ键和π键判断等,难度中等,注意理解杂化轨道理论与价层电子对互斥理论,进行分子构型的判断.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
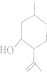
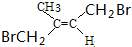
10.已知1,3丁二烯( )可以发生1,2加成或者1,4加成,其1,4加成反应的原理是分子中的两个双键同时断裂,1,4号碳各加上一个原子后,中间两个碳的未成对电子又配对成双键.则有机物A(结构简式
)可以发生1,2加成或者1,4加成,其1,4加成反应的原理是分子中的两个双键同时断裂,1,4号碳各加上一个原子后,中间两个碳的未成对电子又配对成双键.则有机物A(结构简式  )与溴水反应的产物共有( )种.
)与溴水反应的产物共有( )种.
 )可以发生1,2加成或者1,4加成,其1,4加成反应的原理是分子中的两个双键同时断裂,1,4号碳各加上一个原子后,中间两个碳的未成对电子又配对成双键.则有机物A(结构简式
)可以发生1,2加成或者1,4加成,其1,4加成反应的原理是分子中的两个双键同时断裂,1,4号碳各加上一个原子后,中间两个碳的未成对电子又配对成双键.则有机物A(结构简式  )与溴水反应的产物共有( )种.
)与溴水反应的产物共有( )种.| A. | 5 | B. | 8 | C. | 9 | D. | 10 |
14.葡萄糖中含有下列那种官能团( )
| A. | -CHO | B. | -COOH | C. | -NH2 | D. | -COO- |
11.下列有关实验操作,正确的是( )
| A. | 抽滤结束后,不必拆下布氏漏斗,滤液可直接从支管口倒出 | |
| B. | 在“牙膏中某些主要成分的检验”实验中,在牙膏与蒸馏水搅拌、静置分离后的澄清溶液中加入少量的新制Cu(OH)2,当产生绛蓝色沉淀时,说明牙膏中含有甘油 | |
| C. | 做银镜反应实验后,试管内壁上的附着物用浓氨水洗涤 | |
| D. | 减压过滤不宜过滤胶状沉淀或颗粒太小的沉淀,沉淀的颗粒较大时,可用倾析法将固体与溶液分离 |
12.某些芳香烃化合物的分子式均为C7H8O,其中与FeCl3溶液混合后显紫色的符合该分子式的物质有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
 )是合成青蒿素的重要中间体,某小组设计合成M的路线之一如图所示(部分反应条件略去).
)是合成青蒿素的重要中间体,某小组设计合成M的路线之一如图所示(部分反应条件略去).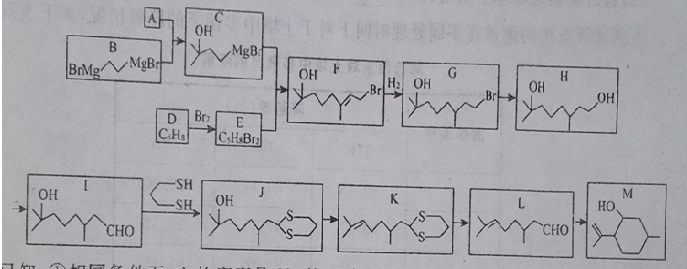
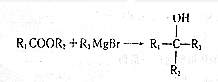
 .
.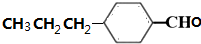 (写出其中任意一种的结构简式).
(写出其中任意一种的结构简式).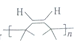 的合成路线2CH3COOCH3+BrMgCH2CH2MgBr→(CH3)C(OH)C(OH)(CH3)2$→_{△}^{浓H_{2}SO_{4}}$CH2=C(CH3)-C(CH3)=CH2$\stackrel{催化剂}{→}$
的合成路线2CH3COOCH3+BrMgCH2CH2MgBr→(CH3)C(OH)C(OH)(CH3)2$→_{△}^{浓H_{2}SO_{4}}$CH2=C(CH3)-C(CH3)=CH2$\stackrel{催化剂}{→}$