题目内容
 如图是元素周期表前四周期的一部分,下列对相关元素的叙述正确的是( )
如图是元素周期表前四周期的一部分,下列对相关元素的叙述正确的是( )| A、X元素的原子有二个电子层,处于周期表的第14纵行 |
| B、X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐 |
| C、Z的原子序数为31,单质常温下为液体 |
| D、气态氢化物水溶液的酸性X<Z<Y |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:如图是元素周期表前四周期的一部分,根据元素在周期表中的位置知,R是He元素、X是N元素、Y是S元素、Z是Br元素,
A.X处于周期表的第15纵行;
B.X的气态氢化物是氨气,Y的最高价氧化物的水化物是硫酸,二者能反应生成盐;
C.Z的原子序数是35;
D.氨气水溶液具有碱性.
A.X处于周期表的第15纵行;
B.X的气态氢化物是氨气,Y的最高价氧化物的水化物是硫酸,二者能反应生成盐;
C.Z的原子序数是35;
D.氨气水溶液具有碱性.
解答:
解:如图是元素周期表前四周期的一部分,根据元素在周期表中的位置知,R是He元素、X是N元素、Y是S元素、Z是Br元素,
A.X是N元素,位于第二周期第VA族,所以X处于周期表的第15纵行,故A错误;
B.X是N元素,X的气态氢化物是氨气,Y的最高价氧化物的水化物是硫酸,二者能反应生成盐,反应方程式为2NH3+H2SO4=(NH4)2SO4,故B正确;
C.Z是Br元素,Z的原子序数是35,溴单质在常温下为液体,故C错误;
D.X的气态氢化物是氨气,氨气水溶液具有碱性,故D错误;
故选B.
A.X是N元素,位于第二周期第VA族,所以X处于周期表的第15纵行,故A错误;
B.X是N元素,X的气态氢化物是氨气,Y的最高价氧化物的水化物是硫酸,二者能反应生成盐,反应方程式为2NH3+H2SO4=(NH4)2SO4,故B正确;
C.Z是Br元素,Z的原子序数是35,溴单质在常温下为液体,故C错误;
D.X的气态氢化物是氨气,氨气水溶液具有碱性,故D错误;
故选B.
点评:本题考查了元素周期表和元素周期律的综合应用,熟悉元素周期表结构并正确推断元素是解本题关键,再结合元素周期律来分析解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法不正确的是( )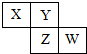
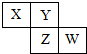
| A、Z元素的原子半径比Y元素的大 |
| B、若Y的最低化合价为-2,则W的最高正化合价为+6 |
| C、若Z的最高正化合价为+5,则X元素的化合物最多 |
| D、若HmZOn为强酸,则Y是活泼非金属元素 |
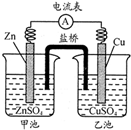 中学教材引入了带盐桥的原电池,该电池即为1806年丹尼尔设计的原电池.如图,下列有关分析正确的是( )
中学教材引入了带盐桥的原电池,该电池即为1806年丹尼尔设计的原电池.如图,下列有关分析正确的是( )| A、负极发生氧化反应:Cu-2e-=Cu2+ |
| B、电池工作时,盐桥逐渐变蓝 |
| C、向乙池中通入H2S后,电池反应停止 |
| D、若将电极Cu改为石墨,电池电流强度发生变化 |
能正确表示下列反应的离子方程式是( )
| A、向氢氧化钠溶液中加入少量铝粉:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| B、NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| C、硫化钠溶液显碱性的原因:S2-+H2O═H2S+2OH- |
| D、向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
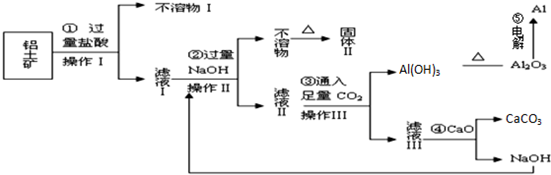
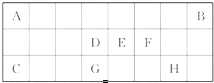 下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.
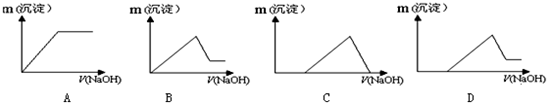
下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.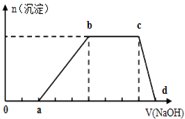 某溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、Cu2+、SO42-、I-、CO32-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知:
某溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、Cu2+、SO42-、I-、CO32-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知: